
ʵ���ҳ�������������Ӧ�Ʊ�Cl2����MnO2��Ũ���ᷴӦ�Ʊ���������2KMnO4+16HCl(Ũ)=2KCl+2MnCl2+5Cl2 +8H2O�� ��KClO3+6HCl(Ũ)=KCl+3Cl2 +3H2O����ֱ������������Ƶõ�����Cl2������˵������ȷ���� ( )
A���μӷ�Ӧ��HCl�����ʵ������
B��ת�Ƶ��ӵ��������
C�����������������ʵ������
D�����������������������
 ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д� Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

| ||
| (һ������) |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
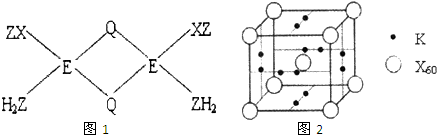 ��֪X��Y��Z��Q��E����Ԫ�ص�ԭ������������������Xԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��s�ܼ���������P�ܼ���������������Zԭ��L������2�ԳɶԵ��ӣ�Q�ǵ��������е縺������Ԫ�أ�E+��M��3d�������ȫ��������ش��������⣺
��֪X��Y��Z��Q��E����Ԫ�ص�ԭ������������������Xԭ�Ӻ��������6�ֲ�ͬ���˶�״̬��s�ܼ���������P�ܼ���������������Zԭ��L������2�ԳɶԵ��ӣ�Q�ǵ��������е縺������Ԫ�أ�E+��M��3d�������ȫ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011���Ĵ�ʡ�����й㺺��ѧ�߿���ѧ��ϰ�Ծ��������棩 ���ͣ������

 2NH3��
2NH3��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com