
| A、热的纯碱溶液和冷的纯碱溶液洗涤油污效果一样好 |
| B、常温下,将氨水加入到盐酸中,所得溶液中一定存在:c(H+)+c(NH4+)=c(Cl-)+c(OH-) |
| C、中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 |
| D、强电解质的水溶液的导电性一定比弱电解质的水溶液强 |


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:

| 选项 | 现象 | 解释或结论 |
| A | a处黄色褪去 | 非金属性:Br>S |
| B | b处变为红色 | 二氧化硫与水反应生成酸性物质 |
| C | c处变为蓝色 | 二氧化硫具有一定的氧化性 |
| D | d处红色先褪去后恢复 | 二氧化硫具有漂白性且漂白性不稳定 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物 |
| B、Na2O2中氧元素的化合价为-2价 |
| C、Na2O与CO2发生化合反应生成Na2CO3,Na2O2与CO2发生置换反应生成O2 |
| D、Na2O2需要密封保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe3+、NH4+、SCN-、Cl- |
| B、Fe2+、NH4+、Cl-、OH- |
| C、Al3+、Na+、OH-、Cl- |
| D、Na+、H+、NO3-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、干冰升华 |
| B、CaCO3(s)分解为CaO(s)和CO2(g) |
| C、NH3(g)与HCl(g)反应生成NH4Cl(s) |
| D、氯化钠溶于水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
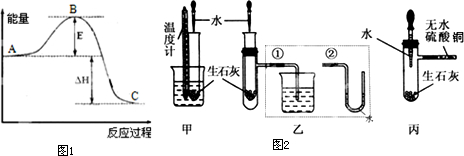
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①⑤ | B、③④⑤ |
| C、①②③⑤ | D、①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com