
| 0.01mol?L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol?L-1 Na2SO3溶液的体积/mL | H2O的体积/mL | 实验温度 /℃ | 溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | t 1 |
| 实验2 | 5 | 5 | 40 | 25 | t2 |
| 实验3 | 5 | 5 | V2 | 0 | t 3 |


科目:高中化学 来源: 题型:
| A、①③④ | B、②⑤ |
| C、②③⑤ | D、①③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 是一种医药中间体,常用来制备抗凝血药,可通过下列流程合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列流程合成:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
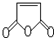 是合成某些药物的中间体.试设计合理方案由化合物
是合成某些药物的中间体.试设计合理方案由化合物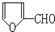 合成
合成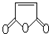 .
.| HBr |
| NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、福尔马林、葡萄糖与银氨溶液共热都有光亮的银镜生成 |
B、有机物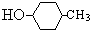 的消去产物有两种 的消去产物有两种 |
| C、鸡蛋清溶液中加入饱和(NH4)2SO4溶液后产生沉淀,是因为蛋白质发生了盐析 |
| D、沾附在试管内壁上的油脂,用热碱液洗涤 |
查看答案和解析>>
科目:高中化学 来源: 题型:
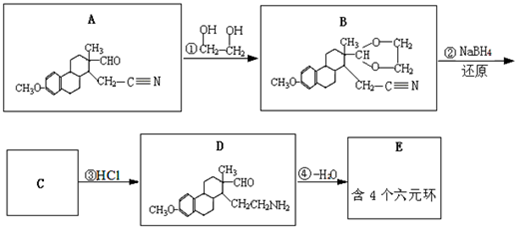
 (提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A→B→C…→H.)
(提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A→B→C…→H.)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com