
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源:不详 题型:单选题
| A.金属钠与O2反应,条件不同,产物不同 |
| B.少量钠可保存在煤油中 |
| C.金属钠质软,可以用小刀切割 |
| D.由于钠很活泼,所以能从水溶液中置换出金属活动性顺序表中排在钠后面的金属单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5∶2 | B.2∶5 | C.2∶1 | D.1∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
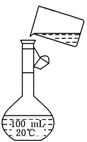

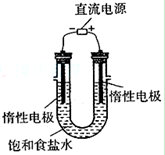
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 2H2O2 →2H2O+ O2↑.为测定已变质的过碳酸钠(含碳酸钠)的纯度,设计如图所示的实验:Q为—具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中。
2H2O2 →2H2O+ O2↑.为测定已变质的过碳酸钠(含碳酸钠)的纯度,设计如图所示的实验:Q为—具有良好的弹性的气球(不与反应物和生成物反应),称取一定量的样品和少量二氧化锰放于其中,按图安装好实验装置,打开分液漏斗的活塞,将稀H2SO4滴入气球中。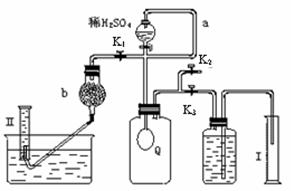
 _________________。
_________________。| A.气体滞留在Q和导气管中,未全部进入量筒Ⅱ |
B.量筒Ⅱ读数时 ,量筒液面高于水槽液面 ,量筒液面高于水槽液面 |
| C.右侧量筒Ⅰ和储液集气瓶连接导管内的液体没有计入读数x |
| D.气体体积数值x、y没有扣除滴加的硫酸的体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
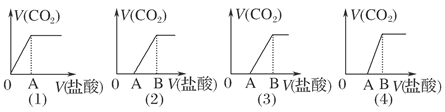
| A.M中只有一种溶质的有(1)和(3) | B.M中有两种溶质的有(2)和(4) |
| C.(2)图显示M中c(NaHCO3)>c(Na2CO3) | D.(4)图显示M中c(NaHCO3)>c(Na2CO3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
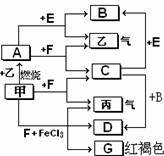
 18号元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)
18号元素组成的一些单质及其化合物之间的转化关系图。常温常压下,D、F、K均为无色无刺激性气味的气体,B是最常见的无色液体,A是由单质C在D中燃烧生成的淡黄色固体。(反应中生成的部分物质已略去)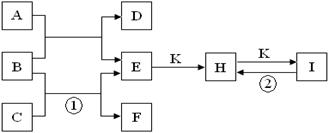
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com