
A. | B. | C. | D. |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.6.02×1023就是阿伏加德罗常数 |
| B.12 g 12C含有的碳原子数就是阿伏加德罗常数 |
| C.含有阿伏加德罗常数个粒子的物质的量就是1 mol |
| D.1 mol氯含有6.02×1023个氯分子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CH4 | B.C2H4 | C.C2H2 | D.C4H10 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
| 气体 | 瓶中气体质量/g | R(%) | 气体 | 瓶中气体质量/g | R% |
| N2 | 0.652 | - | Y | 2.398 | 68.9 |
| X | 0.849 | 97.4 | Z | 3.583 | 92.2 |
| 气体 | 瓶中气体质量/g | R(%) | 气体 | 瓶中气体质量/g | R% |
| N2 | 0.652 | - | Y | 2.398 | 68.9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.5.6 L | B.11.2 L | C.22.4 L | D.33.6 L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
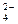 为______________mol。
为______________mol。 H2O+2CuO+CO2↑,则120 ℃时分解产生的混合气体的平均相对分子质量是___________。
H2O+2CuO+CO2↑,则120 ℃时分解产生的混合气体的平均相对分子质量是___________。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com