
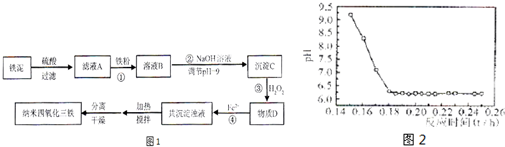
| 2Fe |
| Fe3O4 |
| 2×56 |
| 232 |


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:阅读理解
| 实验序号 | 双氧水(mL) | pH | 反应时间 |
| 1 | 0.5 | 11 | 3 |
| 2 | 0.4 | 11 | 3 |
| 3 | 0.6 | 11 | 3 |
| 4 | 0.5 | 10 | 3 |
| 5 | |||
| 6 | |||
| 7 |
查看答案和解析>>
科目:高中化学 来源:2012届江苏省淮安市范集中学高三第一次全真模拟测试化学试卷(带解析) 题型:填空题
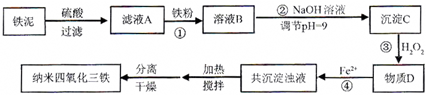
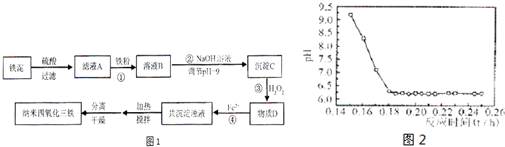
(12分)利用染化厂的废料铁泥(主要成分是Fe2O3、FeO和铁)制备可用于隐形飞机涂层的纳米四氧化三铁的生产流程为:
请回答:
(1)过程①主要反应的离子方程式为 。
(2)已知氢氧化亚铁的Ksp=4.87×10-17,氢氧化铁的Ksp=2.6×10-39。
当溶液中某离子浓度不高于1×10-5 mol·L-1时,可以认为该离子已经完全沉淀。通过计算所得数据说明过程②调节pH=9的原因是 。
(3)物质D的主要产物中铁、氢、氧三种元素的质量比为56∶1∶32,则过程③主要反应的化学方程式为 。
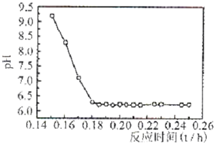
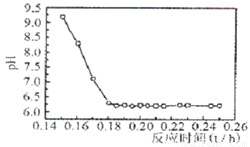
(4)已知Fe2+在弱碱性溶液中还原性较强,图11是研究过程④的实验所得,则该反应所需的时间控制在 小时左右,较为适宜。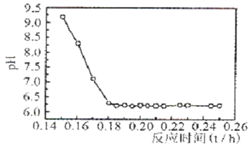
(5)某工厂处理废铁泥(测得铁元素含量为16.8 %)的能力为10吨/小时,生产纳米四氧化三铁的产量为4.64吨/小时。如不考虑过程④以后生产中Fe2+的氧化,则该工厂每小时消耗铁粉的质量为 千克。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江苏省淮安市高三第一次全真模拟测试化学试卷(解析版) 题型:填空题
(12分)利用染化厂的废料铁泥(主要成分是Fe2O3、FeO和铁)制备可用于隐形飞机涂层的纳米四氧化三铁的生产流程为:
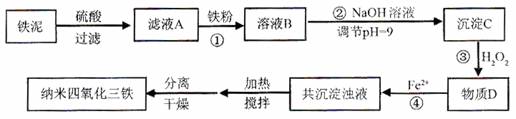
请回答:
(1)过程①主要反应的离子方程式为 。
(2)已知氢氧化亚铁的Ksp=4.87×10-17,氢氧化铁的Ksp=2.6×10-39。
当溶液中某离子浓度不高于1×10-5 mol·L-1时,可以认为该离子已经完全沉淀。通过计算所得数据说明过程②调节pH=9的原因是 。
(3)物质D的主要产物中铁、氢、氧三种元素的质量比为56∶1∶32, 则过程③主要反应的化学方程式为 。
(4)已知Fe2+在弱碱性溶液中还原性较强,图11是研究过程④的实验所得,则该反应所需的时间控制在 小时左右,较为适宜。
(5)某工厂处理废铁泥(测得铁元素含量为16.8 %)的能力为10吨/小时,生产纳米四氧化三铁的产量为4.64吨/小时。如不考虑过程④以后生产中Fe2+的氧化,则该工厂每小时消耗铁粉的质量为 千克。
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com