
(14分)二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料。
Ⅰ.二氧化钛可由以下两种方法制备:
方法1:TiCl4水解生成TiO2·xH2O,过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2,此方法制备得到的是纳米二氧化钛。
(1)①TiCl4水解生成TiO2·xH2O的化学方程式为 。
②检验TiO2·xH2O中Cl-是否被除净的方法是 。
方法2:可用含有Fe2O3的钛铁矿(主要成分为FeTiO3,其中Ti元素化合价为+4价)制取,其主要流程如下:

(2)Fe2O3与H2SO4反应的离子方程式是 。
(3)甲溶液中除含TiO2+之外还含有的金属阳离子有 。
(4)加Fe的作用是 。
Ⅱ、二氧化钛可用于制取钛单质
(5)TiO2制取单质Ti,涉及到的步骤如下:
TiO2 TiCl4
TiCl4 Ti
Ti
反应②的方程式是 ,该反应需要在Ar气氛中进
行,请解释原因: 。
(14分,每空2分)
(1)①TiCl4 + (x + 2)H2O(过量) TiO2·xH2O↓ + 4HCl(写=不扣分)
TiO2·xH2O↓ + 4HCl(写=不扣分)
②取少量水洗液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已洗净。
(2)Fe2O3 + 6H+ = 2Fe3+ + 3H2O
(3)Fe3+、Fe2+
(4)将Fe3+转化为Fe2+
(5)TiCl4 + 2Mg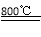 2MgCl2 + Ti;防止高温下Mg(Ti)与空气中O2(或CO2、N2)作用。
2MgCl2 + Ti;防止高温下Mg(Ti)与空气中O2(或CO2、N2)作用。
【解析】
试题分析:(1)①TiCl4水解生成TiO2·xH2O和氯化氢,根据元素守恒规律书写其化学方程式为
TiCl4 + (x + 2)H2O(过量) TiO2·xH2O↓ + 4HCl;
TiO2·xH2O↓ + 4HCl;
②检验沉淀是否被洗干净的方法是取少量洗涤后的溶液,滴加硝酸酸化的AgNO3溶液,不产生白色沉淀,说明Cl-已洗净。
(2)Fe2O3与H2SO4发生反应生成硫酸铁和水,氧化铁是氧化物,不能拆开,硫酸是强酸,写成离子形式,所以离子方程式为Fe2O3 + 6H+ = 2Fe3+ + 3H2O ;
(3)FeTiO3中Ti元素化合价为+4价,则Fe为+2价,钛铁矿中含有氧化铁,所以甲溶液中除iO2+之外还含有的金属阳离子有Fe3+、Fe2+
(4)加Fe的作用是将Fe3+转化为Fe2+,便于Fe2+结晶为FeSO4·7H2O
(5)TiCl4与Mg在800℃发生置换反应生成钛和氯化镁,化学方程式为TiCl4 + 2Mg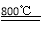 2MgCl2 + Ti;
2MgCl2 + Ti;
Mg与Ti在高温条件下易与空气中的氧气、二氧化碳发生反应,所以为了防止高温下Mg(Ti)与空气中O2(或CO2、N2)作用,该反应需要在Ar气氛中进行。
考点:考查工业制备钛、二氧化钛的反应原理,对工业流程的分析,化学方程式的书写


科目:高中化学 来源:2013-2014北京市丰台区高三二模理综化学试卷(解析版) 题型:简答题
(12分)空气吹出法是最早工业化海水提溴的方法,适合从低浓度含溴溶液中提取溴。

(1)NaBr的电子式是 。
(2)反应①是将Br—转化为Br2,反应①的离子方程式是 。
(3)通入空气吹出Br2,并用Na2CO3吸收的目的是 。
(4)反应②的化学方程式是 。
(5)反应③中每生成3 mol Br2,转移电子的物质的量是 mol。
(6)为了除去工业Br2中微量的Cl2,可向工业Br2中 (填字母)。
a.通入HBrb.加入NaBr溶液 c.加入Na2CO3溶液 d.加入Na2SO3溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014内蒙古鄂尔多斯市高一下学期期末质量检测化学试卷(解析版) 题型:选择题
对于放热反应:H2+Cl2 2HCl,下列说法错误的是
2HCl,下列说法错误的是
A.反应物的总能量大于生成物的总能量
B.该反应遵循“能量守恒定律”
C.该反应中,化学能只转变成热能
D.断开1molH-H键和1molCl-Cl键所吸收的总能量小于形成2molH-Cl键所放出的能量
查看答案和解析>>
科目:高中化学 来源:2013-2014内蒙古赤峰市高三下学期4月统一考试理综化学试卷(解析版) 题型:填空题
(14分)废旧碱性锌锰干电池内部的黑色物质A主要含有MnO2、NH4CI、ZnCI2,还有少量的FeCI2和炭粉,用A制备高纯MnCO3,的流程图如下。

(1)碱性锌锰干电池的负极材料是_________(填化学式)。
(2)第Ⅱ步操作的目的是________________________。
(3)第Ⅳ步操作是对滤液a进行深度除杂,除去Zn2+的离子方程式为____________________。
(已知:Ksp(MnS)=2.5×10-13,Ksp(ZnS)=1.6×10-24)
(4)为选择试剂X,在相同条件下,分别用5 g 黑色物质M进行制备MnSO3的实验,得到数据如右表:
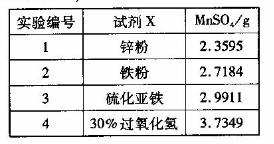
①试剂x的最佳选择是_________。
②第Ⅲ步中用选出的最佳试剂X与M的主要成分反应的化学方程式为_________。
(5)已知:MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解;Mn(OH)2开始沉淀时pH为7.7。请补充完成以下操作:
第Ⅴ步系列操作可按一下流程进行:请补充完成操作:(第Ⅴ步系列操作中可供选用的试剂: 、乙醇)
、乙醇)
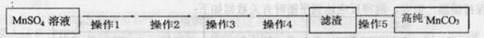
操作1:___________________;操作2:过滤,用少量水洗涤2~3次
操作3:检测滤液,表明SO42-已除干净; 操作4:___________________;
操作5:低温烘干。
(6)操作1可能发生反应的离子方程式
查看答案和解析>>
科目:高中化学 来源:2013-2014内蒙古赤峰市高三下学期4月统一考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.自然界中含有大量的游离态的硅,纯净的硅晶体可用于制作计算机芯片
B.Si、P、S、Cl 相应的最高价氧化物对应水化物的酸性依次增强
C.工业上通常用电解钠、铁、铜对应的氯化物制得该三种金属单质
D.金属铝、铁、铜都有一定的抗腐蚀性能,其抗腐蚀的原因都是表面形成氧化物薄膜,阻止反应的进一步进行
查看答案和解析>>
科目:高中化学 来源:2013-2014内蒙古赤峰市年宁城县高三5月模拟考试理综化学试卷(解析版) 题型:选择题
分子式为C9H18O2的有机物在酸性条件下可水解为酸和醇,且酸与醇的相对分子质量相等。若不考虑立体异构,这些酸和醇重新组合可形成的酯共有
A.12种 B.16种 C.20种 D.24种
查看答案和解析>>
科目:高中化学 来源:2013-2014云南省红河州高三下学期毕业生复习统一检测理综化学试卷(解析版) 题型:填空题
(15分)硬质玻璃管是化学实验中经常使用的一种仪器,请分析下列实验(固定装置略)并回答问题。

Ⅰ、进行微量实验:如图所示,将浓硫酸滴入装有Na2SO3固体的培养皿一段时间后,a、b、c三个棉球变化如下表。请填写表中的空白:
棉球 | 棉球上滴加的试剂 | 实验现象 | 解释和结论 |
a |
| 棉球变白,微热后又恢复红色 |
|
b | 含酚酞的NaOH溶液 | 棉球变为白色 | 离子方程式: |
c |
| 棉球变为白色 | 该气体具有 (选填“氧化性”或“还原性”) |
Ⅱ、硬质玻璃管与其它装置结合完成定性或定量实验。下图是某研究性学习小组对某铁矿石中铁的氧化物的化学式进行探究的装置。

实验一:铁矿石中含氧量的测定
(1)按上图组装仪器(夹持仪器均省略),检查装置的气密性;
(2)将10.0g铁矿石放入硬质玻璃管中;
(3)从左端导气管口处不断地缓缓通入H2, 后,点燃A处酒精灯;
(4)充分反应后,撤掉酒精灯,再持续通入氢气至完全冷却。
(5)测得反应后装置B增重2.70g,则铁矿石中氧的质量分数为______________________。
实验二:铁矿石中含铁量的测定

(1)步骤②和⑤中都要用到的玻璃仪器是 __。
(2)下列有关步骤⑥的操作中说法不正确的是_______。
A.滴定管用蒸馏水洗涤后再用待装液润洗
B.锥形瓶需要用待测液润洗
C.因为碘水为黄色,所以滴定过程中不需加指示剂
实验结论:推算铁的氧化物的组成,由实验一、二得出该铁矿石中铁的氧化物的化学式为
查看答案和解析>>
科目:高中化学 来源:2013-2014云南省高二下学期第二次月考化学试卷(解析版) 题型:选择题
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl。下列“水” 电池在海水中放电时的有关说法正确的是
A.每生成1 mol Na2Mn5O10转移2 mol电子 B.正极反应式:Ag+Cl--e-=AgCl
C.Na+不断向“水”电池的负极移动 D.AgCl是还原产物
查看答案和解析>>
科目:高中化学 来源:2013-2014云南省高一下学期期末考试化学试卷(解析版) 题型:选择题
胶体分散系与其它分散系的本质差别是
A.是否有丁达尔现象B.分散质粒子是否带电
C.是否稳定 D.分散质直径大小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com