
下列化学反应属于放热反应的是 ( )
A.铁跟盐酸反应 B.C和CO2共热
C.碳酸钙的分解 D.Ba(OH)2晶体与NH4Cl晶体反应
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| ||
| TiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

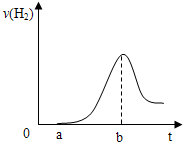
查看答案和解析>>
科目:高中化学 来源: 题型:
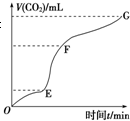 用纯净的碳酸钙粉末跟稀盐酸反应制取二氧化碳气体,请回答:
用纯净的碳酸钙粉末跟稀盐酸反应制取二氧化碳气体,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
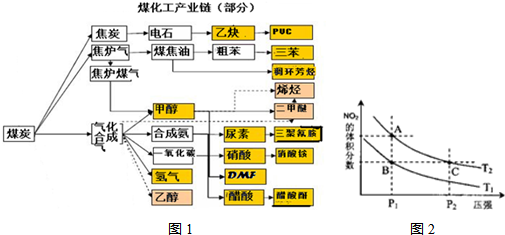
| c(H2)c(CO) |
| c(H2O) |
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
 和
和 .实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式
.实验测得N-N键键能为167kJ?mol-1,NO2中氮氧键的键能为466kJ?mol-1,N2O4中氮氧键的键能为438.5kJ?mol-1.请写出NO2转化为N2O4的热化学方程式查看答案和解析>>
科目:高中化学 来源: 题型:
 (l)+H2(g)-→
(l)+H2(g)-→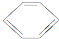 (l)△H>0 ①
(l)△H>0 ①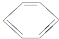 (l)+2H2(g)-→
(l)+2H2(g)-→ (l)△H<0 ②
(l)△H<0 ②| A、反应①、②都属于加成反应 | B、在通常条件下,反应①、②都能自发进行 | C、反应①吸热、反应②放热的事实说明苯环中含有的并不是碳碳双键 | D、反应①、②中的所有有机物均可使溴水褪色,但褪色原理不完全相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com