
分析 (1)根据基态原子的电子排布式来解答;
(2)在原子中,核电荷数=核内质子数=核外电子数,B元素原子的核电荷数为n,B得到1个电子后变为B-,C失去1个电子后变为C+,根据电子层结构相同,即核外电子数相同,列出等式求解即可;
(3)D元素的正三价离子的3d轨道为半充满,3d轨道电子数为5,应为Fe元素.
解答 解:(1)基态原子的最外层有3个未成对电子,次外层有2个电子的元素符号为N,其电子排布式为:1s22s22p3,故答案为:N;
(2)设元素B的核电荷数是a,C元素原子的核电荷数为b,因为阴离子B-与阳离子C+电子层结构都与氩相同相同,即核外电子数相同,所以a=18-1=17,b=18+1=19,所以B是Cl,C为K原子,故答案为:Cl;K;
(3)D元素的正三价离子的3d轨道为半充满,3d轨道电子数为5,则基态原子的电子排布式为1s22s22p63s23p63d64s2,应为Fe元素,故答案为:Fe;1s22s22p63s23p63d64s2.
点评 本题考查元素推断题,题目难度中等,推断元素的种类为该题的关键,注意相关知识的积累,把握原子结构的相关规律.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:选择题
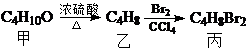 ;丙不可能是( )
;丙不可能是( )| A. | CH3CH2CHBrCH2Br | B. | (CH3)2CBrCH2Br | C. | CH3CHBrCHBrCH3 | D. | CH3CH (CH2Br)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若完全燃烧,1 mol雌酮(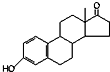 )比雄酮( )比雄酮(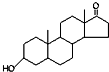 )多消耗3 mol O2 )多消耗3 mol O2 | |
| B. | 正戊烷、异戊烷和新戊烷互为同分异构体,沸点依次升高 | |
| C. | 甲醛、甲酸、甲酸钠,均能发生银镜反应 | |
| D. | 乙醇依次通过消去、取代、加成反应可生成乙二醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
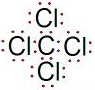 ,空间构型为正四面体.
,空间构型为正四面体.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ③④⑤ | C. | ②③⑤ | D. | ①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 放热反应一定是断开反应物中的化学键吸收的能量比形成生成物中的化学键放出的能量少 | |
| B. | 1molH2SO4和1molBa(OH)2完全反应所放出的热量称为中和热 | |
| C. | 反应物的总能量低于生成物的总能量的化学反应为放热反应 | |
| D. | 在化学反应中需要加热的反应就是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 它们的原子核外电子层数随核电荷数的增加而增多 | |
| B. | 它们的熔沸点随核电荷数的增加而增加 | |
| C. | 它们的氢化物的稳定性随核电荷数的增加而增强 | |
| D. | 单质的颜色随核电荷数的增加而加深 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
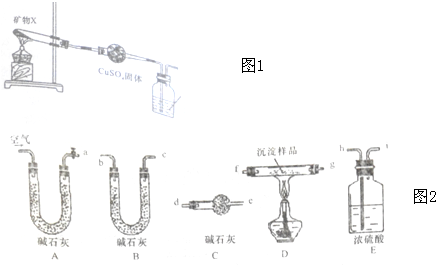
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com