
【题目】化合物A[KxFe(C2O4)y·zH2O,其中铁元素为+3价]是一种重要的光化学试剂。
(1)制备化合物A的实验流程如下:
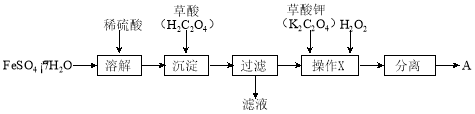
① 上述流程中,检验“过滤”后的固体已洗涤干净的方法是 。
② 上述流程“操作X”中加入H2O2的目的是 。
(2)测定化合物A的化学式实验步骤如下:
a、准确称取A样品4.91g,干燥脱水至恒重,残留物质的质量为4.37g;
b、将步骤a所得固体溶于水,加入还原铁粉0.28g,恰好完全反应;
c、另取A样品4.91g置于锥形瓶中,加入足量的3 mol/L的H2SO4溶液和适量蒸馏水,再加入0.50mol/L的KMnO4溶液24.0 mL,微热,恰好完全反应:
2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O
通过计算填空,请写出解题过程。
① 4.91g A样品中含结晶水的物质的量为 mol。
② A样品中![]() = 。
= 。
③ A的化学式为 。
【答案】(1)① 取少量最后一次洗涤液于试管中,滴加BaCl2溶液,无白色沉淀,说明已洗涤干净。(2分)② 把Fe2+全部氧化成Fe3+
(2)①0.03(2分)②1:3(2分)③K3Fe(C2O4)3·3H2O(4分)
计算过程:n(H2O)=![]()
n(Fe3+)=2n(Fe)=![]()
n(C2O42-)=![]() n(KMnO4)=
n(KMnO4)=![]() ×0.50molL-1×0.024L=0.03mol
×0.50molL-1×0.024L=0.03mol
![]() =1:3
=1:3
根据离子电荷守恒:n(K+)+3n(Fe3+)=2n (C2O42-)得n(K+)=0.03mol
因此A为 K3Fe(C2O4)3·3H2O
【解析】
试题分析:(1)① 滤液中含有硫酸根,因此可以通过检验洗涤液中是否含有硫酸根判断是否洗涤干净。即取少量最后一次洗涤液于试管中,滴加BaCl2溶液,无白色沉淀,说明已洗涤干净。
②由于铁元素最终必需转化为铁离子,所以双氧水的作用是把Fe2+全部氧化成Fe3+。
(2)①样品中结晶水的物质的量n(H2O)=![]() ;
;
②n(Fe3+)=2n(Fe)=![]()
根据反应的方程式可知n(C2O42-)=![]() n(KMnO4)=
n(KMnO4)=![]() ×0.50molL-1×0.024L=0.03mol
×0.50molL-1×0.024L=0.03mol
所以![]() =1:3
=1:3
③根据离子电荷守恒n(K+)+3n(Fe3+)=2n (C2O42-)可得n(K+)=0.03mol
因此A为 K3Fe(C2O4)3·3H2O


 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 烷烃可与溴水发生加成反应
B. 酚酞溶液可鉴别乙醇和乙酸
C. 酒精不可萃取碘水中的碘单质
D. 聚丙烯可使酸性高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是
A.间二甲苯也叫1,5-二甲苯
B.可用氢氧化钠溶液除去乙酸乙酯中残留的乙酸
C.C6H14有5种同分异构体
D.乙醇转化为乙醛和乙醇直接转化为乙酸的反应类型不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将碘水倒入汽油中,下列现象描述正确的是
A.汽油在上层,水在下层,汽油无色
B.汽油在下层,水在上层,汽油紫色
C.汽油在上层,水在下层,水无色。
D.汽油在上层,水在下层,汽油紫色。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mL某浓度的硫酸溶液中滴入0.1mol/L氨水,溶液中水电离的氢离子浓度随加入氨水的体积变化如图。下列分析正确的是( )
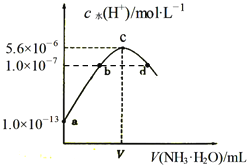
A. V=40
B. c点所示溶液中:c(H+ )-c(OH-)=2c(NH3·H2O)
C. NH3·H2O的电离常数K=10-4
D. d点所示溶液中:c(NH4+)=2c(SO42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】23.75 g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量为________, MCl2的相对分子质量为________,M的相对原子质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A.粗盐提纯蒸发时,待水分完全蒸干后停止加热
B.过滤时,漏斗下口尖端紧贴烧杯内壁
C.蒸馏时,冷却水应从冷凝管上口进下口出
D.分液操作时,上层液体应从分液漏斗下口放出
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com