
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:阅读理解
| ||
查看答案和解析>>
科目:高中化学 来源:2010—2011学年辽宁省沈阳二中高二下学期期末考试化学试卷 题型:单选题
a、b、c、d是四种短周期元素。a、b、d同周期,c、d同主族且c比d少一个电子层。a的原子结构示意图如下左图,b与c形成化合物的电子式如下右图。下列比较中正确的是


| A.原子半径b>a>d | B.单质的氧化性a>c>d |
| C.最高价氧化物的熔点a>d>b | D.最高价含氧酸的酸性d>c>a |
查看答案和解析>>
科目:高中化学 来源:2015届四川省资阳市高一下学期期末检测化学试卷(解析版) 题型:选择题
下列比较中正确的是
A.金属性:Mg>Al>Na B.原子半径:S>O>F
C.碱性:KOH>Mg(OH)2>NaOH D.氢化物的稳定性:HBr>HCl>PH3
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高一下学期期中考试化学试卷 题型:选择题
a、b、c、d是四种短周期元素,a、b、d同周期,c、d同主族。a的原子结构示意图为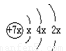 ,b与c形成的化合物为 b3c,其中b的化合价为+1。下列比较中正确的是
,b与c形成的化合物为 b3c,其中b的化合价为+1。下列比较中正确的是
A.原子半径:a>c>d B.单质的氧化性:a>c>d
C.原子序数:a>d>b>c D.最高价含氧酸的酸性:c>d>a
查看答案和解析>>
科目:高中化学 来源:2012届山东省高二下学期第一次月考化学试卷 题型:选择题
a、b、c、d是四种短周期元素。a、b、d同周期, c、d同主族。a的原子结构示意图为 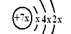 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为 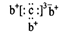 。下列比较中正确的是
。下列比较中正确的是
A.原子半径:a>c>d>b B.电负性a>b>d>c
C.原子序数:d>a>c>b D.最高价含氧酸的酸性c>d>a
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com