
【题目】下列指定反应的离子方程式正确的是( )
A. 向稀HNO3中滴加Na2SO3溶液:SO![]() +2H+===SO2↑+H2O
+2H+===SO2↑+H2O
B. NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:
Al3++2SO42-+2Ba2++4OH-= AlO2-+2BaSO4↓+2H2O
C. 酸性溶液中KIO3与KI反应生成I2:IO+I-+6H+===I2+3H2O
D. 用高锰酸钾标准溶液滴定草酸钠:2MnO+16H++5C2O![]() ===2Mn2++10CO2↑+8H2O
===2Mn2++10CO2↑+8H2O
【答案】D
【解析】A、 HNO3有强的氧化性,Na2SO3有还原性,两者会发生氧化还原反应,离子方程式是:2H++2NO3-+3SO32-=H2O+3SO42-+2NO↑,选项A错误;A、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀,两者物质的量之比是1:2;离子方程式为:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+2BaSO4↓++NH3H2O,选项B错误;C、电荷不守恒,离子方程式应该为:IO3-+5I-+6H+=3I2+3H2O,选项C错误;D、用高锰酸钾标准溶液滴定草酸钠,高锰酸根离子被还原为锰离子,草酸根离子被氧化为二氧化碳,反应的离子方程式为:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O,选项D正确。答案选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子被称为活化分子.使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJmol﹣1表示.请认真观察如图,然后回答问题. 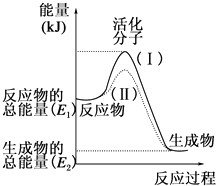
(1)图中所示反应是(填“吸热”或“放热”)反应.
(2)已知拆开1mol H﹣H键、1mol I﹣I、1mol H﹣I键分别需要吸收的能量为436kJ、151kJ、299kJ.则由1mol氢气和1mol 碘反应生成HI会(填“放出”或“吸收”)kJ的热量.在化学反应过程中,是将转化为 .
(3)下列反应中,属于放热反应的是 , 属于吸热反应的是 .
①物质燃烧
②炸药爆炸
③酸碱中和反应
④二氧化碳通过炽热的碳
⑤食物因氧化而腐败
⑥Ba(OH)28H2O与NH4Cl反应
⑦铁粉与稀盐酸反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用过量氢氧化钠溶液处理铝土矿并过滤,得到含偏铝酸钠的溶液。向该溶液中通入二氧化碳,已知通入二氧化碳336L(标准状况下),生成24molAl(OH)3和15molNa2CO3,若通入溶液的二氧化碳为112L(标准状况下),生成Al(OH)3的和Na2CO3的物质的量之比为( )
A. 2:1 B. 1:2 C. 5:4 D. 4:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LiAlH4( )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是( )
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125℃分解为LiH、H2和Al。下列说法不正确的是( )
A. 1 mol LiAlH4在125℃完全分解,转移3 mol电子
B. LiH与D2O反应,所得氢气的摩尔质量为4 g/mol
C. LiAlH4溶于水得到无色溶液,化学方程式可表示为:LiAlH4 + 2H2O![]() LiAlO2 + 4H2↑
LiAlO2 + 4H2↑
D. LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的溶液加热、蒸发、浓缩、结晶、灼烧,所得固体的成分不相同的是( )
A.FeCl 2、FeCl 3 B.NaHCO3、Na2CO3
C.NaAlO2、AlCl3 D.Mg(HCO3)2、MgCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
实验编号 | 反应物 | 催化剂 |
① | 10 mL 2% H2O2溶液 | 无 |
② | 10 mL 5% H2O2溶液 | 无 |
③ | 10 mL 5% H2O2溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
④ | 10 mL 5% H2O2溶液+少量HCl溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
⑤ | 10 mL 5% H2O2溶液+少量NaOH溶液 | 1 mL 0.1 mol·L-1 FeCl3溶液 |
(1)催化剂能加快化学反应速率的原因是_________________________________________。
(2)H2O2分解的化学方程式为________________________。
(3)实验①和②的目的是_______________________________________________________。
实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是______________________________。
(4)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图:
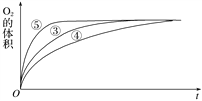
分析上图能够得出的实验结论是_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com