
【题目】铁是生活中的一种常见金属,用途非常广泛.
(1)FeCl3溶液用于腐蚀印刷线路板,反应的离子方程式为
(2)用废铁皮制取铁红粉的局部流程图如下:
①步骤I温度不能太高的原因是
②步骤Ⅱ中发生反应:
4Fe(NO3)2+O2+(2n+4)H2O═24Fe2O3H2O+8HNO3
4Fe+10HNO3═4Fe(NO3)2+NH4NO3+3H2O
第一个反应的氧化剂是
笫二个反应每生成1molNH4NO3 , 转移的电子数是
③铁红可用于焊接钢轨,其反应的化学方程式为
④上述生产结束后,流程中氮元素最主要的存在形式为(填字母)
a.氮氧化物 b.硝酸按 c.硝酸亚铁 d.硝酸.
【答案】
(1)2Fe3++Cu=2Fe2++Cu2+
(2)温度太高硝酸易分解;O2;8NA;Fe2O3+2Al ![]() Al2O3+2Fe;b
Al2O3+2Fe;b
【解析】解:(1)工业上用FeCl3溶液与铜发生氧化还原反应生成氯化亚铁和氯化亚铜这一原理来腐蚀印刷线路,反应的离子方程式为2Fe3++Cu=2Fe2++Cu2+ , 所以答案是:2Fe3++Cu=2Fe2++Cu2+;(2)由流程图可知,Fe与硝酸反应生成硝酸亚铁,步骤Ⅱ中转化为Fe2O3nH2O,最后得到铁红,①硝酸受热易分解,所以步骤I温度不能太高,所以答案是:温度太高硝酸易分解;②在反应4Fe(NO3)2+O2+(2n+4)H2O═2Fe2O3nH2O+8HNO3中,O元素的化合价从0价变为﹣2价,所以反应的氧化剂是O2 , 根据反应4Fe+10HNO3═4Fe(NO3)2+NH4NO3+3H2O可知,氮从+5价降到﹣3价,反应中共转移8个电子,所以每生成1molNH4NO3 , 转移8NA个电子,所以答案是:O2;8NA;③铁红发生铝热反应,可用于焊接钢轨,其反应的化学方程式为Fe2O3+2Al ![]() Al2O3+2Fe,所以答案是:Fe2O3+2Al
Al2O3+2Fe,所以答案是:Fe2O3+2Al ![]() Al2O3+2Fe;④根据流程图可知,生产结束后氮元素主要存在硝酸铵溶液中,所以答案是:b.
Al2O3+2Fe;④根据流程图可知,生产结束后氮元素主要存在硝酸铵溶液中,所以答案是:b.


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】今有两个氢气燃烧生成水的热化学方程式:H2(g)+1/2O2(g)═H2O(g)△H=akJ/mol
2H2(g)+O2(g)═2H2O(l)△H=bkJ/mol
请回答下列问题:(提示:|b|表示b的绝对值)
(1)若2molH2完全燃烧生成水蒸气,则放出的热量|b|kJ(填“>”、“<”或“=”)
(2)反应热的关系:2ab(填“>”、“<”或“=”).
(3)若已知H2(g)+1/2O2(g)═H2O(g)△H=﹣242kJ/mol,且氧气中1mol O=O键完全断裂时吸收热量496kJ,水蒸气中1mol H﹣O键形成时放出热量463kJ,则氢气中1molH﹣H键断裂时吸收的热量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,下列选项中括号内的物质能被完全消耗的是( )
A.常温下将64g铜片投人过量浓硫酸中(铜片)
B.向含有0.2molBa(OH)2和0.lmolNaOH的混合溶液中通人标况下3.36LCO2(CO2)
C.向l0mL3molL﹣1的盐酸中加人5.6g铁(铁)
D.向5.5gMnO2粉末中加人20mL2molL﹣1双氧水(MnO2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有显著抗癌活性的10﹣羟基喜树碱的结构如图所示.下列关于10﹣羟基喜树碱的说法正确的是( ) 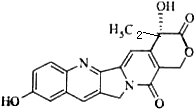
A.分子式为C20H16N2O5
B.不能与FeCl3溶液发生显色反应
C.不能发生酯化反应
D.一定条件下,1mol该物质最多可与1mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 1mol H2SO4的质量为98gmol-1 B. SO3的摩尔质量为80gmol-1
C. 1molO就是1mol 氧气 D. SO2 的摩尔质量与其相对分子质量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,完成题目:
(1)请写出下列反应对应的离子方程式: ①用盐酸中和氢氧化钠溶液: .
②用稀硫酸清洗铁锈(Fe2O3):;
(2)写出离子反应方程式所对应的一个化学方程式.①Ba2++2OH﹣+SO ![]() +2H+=BaSO4↓+2H2O
+2H+=BaSO4↓+2H2O
②CO ![]() +2H+=H2O+CO2↑ .
+2H+=H2O+CO2↑ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用 X 射线对 BaSO4 穿透能力较差的特性,医学上在进行消化系统的 X 射线透视时,常用 BaSO4 作内服造影剂,这种检查手段称为钡餐透视.
(1)医学上进行钡餐透视时为什么不用 BaCO3?(用离子方程式表示)________________________________
(2)某课外活动小组为了探究 BaSO4 的溶解度,分别将足量 BaSO4 放入a.5mL 水 ;b.40mL 0.2molL-1Ba(OH)2 溶 液 c.20mL 0.5molL-1Na2SO4 溶 液 d.40mL 0.1molL-1H2SO4溶液中,溶解至饱和。
①以上各溶液中,Ba2+的浓度由大到小的顺序为_______________________________
A.b>a>c>d B.b>a>d>c C.a>d>c>b D.a>b>d>c
②已知 25℃时,Kap=1.1×10-10,上述条件下,溶液 b 中的 SO42-浓度为_________________molL-1,溶解 c中 Ba2+的浓度为_________________molL-1
③某同学取同体积的溶液 b 和溶液 d④直接混合,则混合液的 pH 为_________________(设混合溶液的体积为混合前两溶液的体积之和)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)0.4mol氨气和0.2mol硫化氢的质量之比为 , 所含分子数之比为 .
(2)现有NH3、H2S、HCl三种气体,它们分别都含有1mol氢原子,则三种气体的物质的量之比为 .
(3)以下物质:①碳酸钾 ②空气 ③二氧化碳 ④铜 ⑤食盐 ⑥氢氧化钠 ⑦硫酸铜溶液 ⑧酒精 ⑨蔗糖(C12H22O11).其中属于电解质的是(填序号).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由2﹣氯丙烷制取少量的1,2﹣丙二醇 ![]() 时,需要经过下列哪几步反应( )
时,需要经过下列哪几步反应( )
A.消去、加成、取代
B.加成、消去、取代
C.取代、消去、加成
D.消去、加成、消去
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com