
【题目】已知w g液态苯(C6H6)完全燃烧生成2 mol CO2气体和1 mol液态水,并放出m kJ的热量,下列能正确表示苯燃烧热的热化学方程式的是( )
A. 2C6H6(l)+15O2(g) ===12CO2(g)+6H2O(l) ΔH=-2m kJ·mol-1
B. ![]() C6H6(l)+
C6H6(l)+![]() O2(g)===2CO2(g)+H2O(g) ΔH=-m kJ·mol-1
O2(g)===2CO2(g)+H2O(g) ΔH=-m kJ·mol-1
C. C6H6(l)+![]() O2(g)===6CO2(g)+3H2O(g) ΔH=-m kJ·mol-1
O2(g)===6CO2(g)+3H2O(g) ΔH=-m kJ·mol-1
D. C6H6(l)+![]() O2(g)===6CO2(g)+3H2O(l) ΔH=-3m kJ·mol-1
O2(g)===6CO2(g)+3H2O(l) ΔH=-3m kJ·mol-1
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯
已知: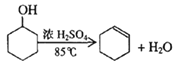


(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入块状物质,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①块状物质的作用是___________,导管B的作用是___________。
②试管C置于冰水浴中的目的是____________________________________。
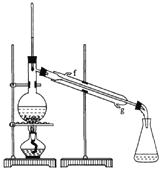
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_________层(填上或下),分液后用_________ (填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按右图装置蒸馏,冷却水从_______口流出,目的是_________
③收集产品时,控制的温度应在_________左右,实验制得的环己烯精品质量低于理论产量,可能的原因是___________
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是_______________________。
a.用酸性高锰酸钾溶液 b.用金属钠 c.测定沸点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某溶液中由水电离产生的c(H+)=1×10-10 mol·L-1,该溶液的溶质不可能是( )
A.NaHSO4B.NaClC.HClD.Ba(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中含原子数最多的是
A. 4℃时5.4mL水 B. 标准状况下5.6L二氧化碳
C. 0.4mol氧气 D. 3.602×1023个氖分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行:Cd+2NiO(OH)+2H2O![]() Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
(1)若用此电池作电源电解足量的M(NO3)x溶液(用碳棒作电极材料),电解池的阳极应连接________(填序号)
①NiO(OH) ②Cd ③Cd(OH)2 ④Ni(OH)2
电池的负极反应为 ___________________。当该电池工作一段时间后消耗了3.6gH2O时,电解池某极增重m g,则金属M的相对原子质量为________________(用m、x表示)。
(2)若用此电池作电源电解含有0.1molCuSO4和0.1molNaCl的混合溶液100mL(用碳棒作电极材料),当电路中有0.2mole-通过时,阳极产生气体__________升(标准状况)。电解后溶液加水稀释至1L,常温下溶液的pH是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为配制250mL 0.2molL﹣1 Na2CO3溶液 的示意图. 
回答下列问题:
(1)①中称得Na2CO3g.
(2)玻璃棒在②、③两步中的作用分别是、 .
(3)第⑧步的操作名称是 .
(4)所用仪器中,除托盘天平、量筒、烧杯、玻璃棒、胶头滴管外,还需要的一种玻璃仪器是 .
(5)若出现如下情况,对所配溶液浓度有何影响?(填“偏高”“偏低”或“无影响”)
A.某同学在第⑧步观察液面时俯视;
B.没有进行操作步骤④和⑤;
C.在第⑤步不慎有少量液体流到容量瓶外 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(多选)下列物质在水溶液中发生电离,其电离方程式正确的是( )
A.Ca(HCO3)2═Ca2++2HCO3﹣
B.KHSO4=K++HSO4﹣
C.Na2SO4═2Na++SO ![]()
D.BaCl2=Ba2++Cl2﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将3.2 g Cu投入100 mL稀硫酸中加热,没有明显变化,若边加热边缓缓加入一定量H2O2,金属Cu逐渐溶解,则下列说法正确的是( )
A. 反应过程中有刺激性气味的气体生成
B. H2O2对Cu和稀硫酸的反应起催化作用
C. 若Cu和硫酸恰好完全反应,则稀硫酸的物质的量浓度为0.5 mol·L-1
D. 反应中硫酸既表现出酸性又表现出氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验需要0.1molL﹣1的 NaOH溶液500mL,其操作有以下各步:
①用托盘天平称量NaOH的质量
②洗涤烧杯和玻璃棒2﹣3次,将洗涤液转入容量瓶中
③将冷却后的氢氧化钠溶液转移入容量瓶中
④将NaOH倒入烧杯中用水溶解、冷却
⑤加水至液面接近刻度线1~2cm处,定容,摇匀
完成下列填空:
(1)实验中除了托盘天平、烧杯、玻璃棒外还需要的其他仪器有 .
(2)根据计算得知,所需NaOH的质量为g.
(3)正确的操作顺序是(用序号填写)
(4)配制过程中,下列情况会使配制结果偏低的是 .
①定容时俯视刻度线观察液面
②未经冷却就进行转移操作
③移液时未洗涤烧杯和玻璃棒
④定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度线.
(5)若取50.0mL上述已配好的溶液,与另一150mL0.2mol/L的NaOH溶液混合,最后得到的溶液的物质的量浓度为(设溶液的体积变化可忽略).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com