
���� ��1������ƽ�ⳣ������д������ʽ����Ӧ�Ƿ��ȷ�Ӧ�����£�ƽ��������У�ƽ�ⳣ����С��
��2���ı���������Ӧ���ʣ����Բ�ȡ������������¡���ѹ������Ũ�ȵȴ�ʩ�������CO��ת����Ӧʹƽ��������Ӧ�����ƶ������ƽ���ƶ�ԭ���������
��3������һ���¶��£����ݻ�Ϊ1L���ܱ������г���3mol H2��3mol CO��������Ӧ��3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g������10minʱ�պôﵽƽ�⣬��ʱ���H2�����ʵ���Ũ��Ϊ1.5mo1•L-1�����ʵ���1.5mo1•L-1��1L=1.5mol��
3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g��
��ʼ����mol�� 3 3 0 0
�仯����mol�� 1.5 1.5 0.5 0.5
ƽ������mol�� 1.5 1.5 0.5 0.5
ת����=$\frac{������}{��ʼ��}$��100%��
�����ݢټ���ƽ�ⳣ���������ʱ��Ũ���̺�ƽ�ⳣ���Ƚϴ�С�жϷ�Ӧ���еķ���
�۸��ݻ�ѧƽ��״̬��������𣬵���Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ������ʵ�Ũ�ȡ��ٷֺ������䣬�Լ��ɴ�������һЩ��Ҳ�������仯������ʱҪע�⣬ѡ���жϵ������������ŷ�Ӧ�Ľ��з����仯�������������ɱ仯����ֵʱ��˵�����淴Ӧ����ƽ��״̬��
��� �⣺��1���÷�Ӧ��ƽ�ⳣ��K=$\frac{c��C{H}_{3}OC{H}_{3}��c��C{O}_{2}��}{{c}^{3}��{H}_{2}��{c}^{3}��CO��}$����Ӧ�Ƿ��ȷ�Ӧ�����£�ƽ��������У�ƽ�ⳣ����С���ʴ�Ϊ��$\frac{c��C{H}_{3}OC{H}_{3}��c��C{O}_{2}��}{{c}^{3}��{H}_{2}��{c}^{3}��CO��}$����С��
��2��a������ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ���CO��ת����������Ӧ���ʼ�С����a����
b�������������Ӧ��������Ӱ��ƽ���ƶ���CO��ת���ʲ��䣬��b����
c������ӦΪ���������С�ķ�Ӧ����С���������ѹǿ����Ӧ��������ƽ��������Ӧ�����ƶ���CO��ת��������c��ȷ��
d������H2��Ũ�ȣ���Ӧ��������ƽ��������Ӧ�ƶ���CO��ת��������d��ȷ��
e������CO��Ũ�ȣ���Ӧ��������ƽ��������Ӧ�ƶ�����CO��ת���ʼ�С����e����
�ʴ�Ϊ��cd��
��3������һ���¶��£����ݻ�Ϊ1L���ܱ������г���3mol H2��3mol CO��������Ӧ��3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g������10minʱ�պôﵽƽ�⣬��ʱ���H2�����ʵ���Ũ��Ϊ1.5mo1•L-1�����ʵ���1.5mo1•L-1��1L=1.5mol��
3H2��g��+3CO��g��?CH3OCH3��g��+CO2��g��
��ʼ����mol�� 3 3 0 0
�仯����mol�� 1.5 1.5 0.5 0.5
ƽ������mol�� 1.5 1.5 0.5 0.5
��ʱn��CH3OCH3��=0.5mol��
ƽ��ʱCO��ת����=$\frac{1.5mol}{3mol}$��100%=50%��
�ʴ�Ϊ��0.5��50%����
��ƽ�ⳣ��K=$\frac{0.5��0.5}{1��{5}^{3}��1��{5}^{3}}$=0.022���ﵽƽ��������������ٳ���1mol H2��1mol CO2��Qc=$\frac{1.5��0.5}{2��{5}^{3}��1��{5}^{3}}$=0.014��K����Ӧ������У�v��������v���棩��
�ʴ�Ϊ������
��A����Ӧ����֮�ȵ��ڻ�ѧ����ʽ������֮�ȣ����κ�ʱ��Ӧ����v��CO��=3v��CO2��������֤����Ӧ�ﵽƽ��״̬����A����
B�����κ�ʱ������amolCO2��ͬʱ����3amolH2��˵����Ӧ������У�����֤����Ӧ�ﵽƽ��״̬����B����
C��c��CO2��=c��CO��������ʼ�����仯���йأ�����֤����Ӧ�ﵽƽ��״̬����C����
D����Ӧǰ�������������䣬�������ʵ�����С����Ӧ�����л�������ƽ����Է����������䣬˵����Ӧ�ﵽƽ��״̬����D��ȷ��
E�����������ܱ������У������������䣬����������仯������������ܶ�ʼ�ղ��䣬����˵����Ӧ�ﵽƽ��״̬����E����
F���ܱ���������������ʼ�ղ��䣬������������������ٸı䣬����˵����Ӧ�ﵽƽ��״̬����F����
�ʴ�Ϊ��D��
���� �����ۺϿ��鷴Ӧ�ȼ��㡢��ѧƽ��Ӱ�����ء���ѧƽ�����ȣ�Ϊ�߿��������ͣ�������ѧ���ķ��������������Ŀ��飬�Ѷ��еȣ�ע��ƽ�ⳣ����Ũ���̱Ƚ��жϷ�Ӧ���з���ķ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ca2+��Na+��SO42-��CO32- | B�� | K+��Fe2+��SO42-��MnO4- | ||
| C�� | Ba2+��K+��Al3+��Cl- | D�� | Na+��Ba2+��Cl-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
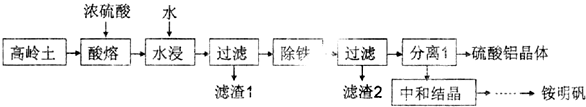
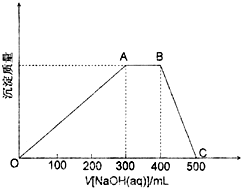
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
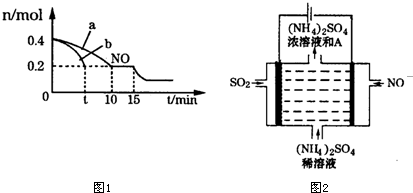
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
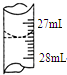 ���ⶨijNaOHmol•L-1��Һ�����ʵ���Ũ�ȣ�����0.100��HCl����Һ�����к͵ζ����ü�����ָʾ������
���ⶨijNaOHmol•L-1��Һ�����ʵ���Ũ�ȣ�����0.100��HCl����Һ�����к͵ζ����ü�����ָʾ������| ʵ����� | ����NaOH��Һ�����/mL | 0.1000mol•L-1HCl��Һ�����/mL | |
| �ζ�ǰ�̶� | �ζ���̶� | ||
| 1 | 25.00 | 0.00 | 26.29 |
| 2 | 25.00 | 1.00 | 31.00 |
| 3 | 25.00 | 1.00 | 27.31 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�22.4 L H2��Cl2�Ļ�������к��еķ�����Ϊ2NA | |
| B�� | �ڱ�״���£�1 mol H2O�����������22.4 L | |
| C�� | ���¶ȸ���0��ʱ��һ�����κ���������������22.4 L | |
| D�� | ����£�ij��������Ϊ22.4 L�������������ʵ���Ϊ1 mol�������ķ�����ĿԼΪ��6.02��1023 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com