
(6分)某元素的同位素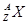 ,它的氯化物XCl2 1.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
,它的氯化物XCl2 1.11g溶于水制成溶液后,加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
(1)Z值和A值;
(2)X元素在周期表中的位置;
(3)写出XCl2的电子式。
科目:高中化学 来源: 题型:
(1)Z值和A值。??????
(2)X元素在周期表中的位置。??????
(3)把X的单质放入水中,有何现象?写出反应的化学方程式。??????
查看答案和解析>>
科目:高中化学 来源: 题型:
(8分)某元素的同位素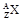 ,它的氯化物XCl21.11g溶于水制成溶液后, 加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
,它的氯化物XCl21.11g溶于水制成溶液后, 加入1mol/L的AgNO3溶液20mL恰好完全反应。若这种同位素原子核内有20个中子,求:
(1)Z值 ▲ 和A值 ▲ ;
(2)X元素在周期表中的位置 ▲ ;
(3)写出XCl2的电子式 ▲ 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省雅安中学高一4月月考化学试卷(带解析) 题型:填空题
某元素的同位素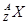 ,它的氯化物XCl2 2.22g溶于水制成溶液后,加入2mol/L的
,它的氯化物XCl2 2.22g溶于水制成溶液后,加入2mol/L的
AgNO3溶液20ml恰好完全反应,若这种同位素原子核内有20个中子,求:
(1)A=
(2)X元素在周期表中的位置? ,XCl2的化学式: 。
查看答案和解析>>
科目:高中化学 来源:2015届四川省高一4月月考化学试卷(解析版) 题型:填空题
某元素的同位素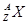 ,它的氯化物XCl2
2.22g溶于水制成溶液后,加入2mol/L的
,它的氯化物XCl2
2.22g溶于水制成溶液后,加入2mol/L的
AgNO3溶液20ml恰好完全反应,若这种同位素原子核内有20个中子,求:
(1)A=
(2)X元素在周期表中的位置? ,XCl2的化学式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com