
【题目】部分被氧化的Fe﹣Cu合金样品(氧化产物为Fe2O3、CuO)共5.92g,经如图处理:
下列说法正确的是( )
A.滤液A中的阳离子为Fe2+、Fe3+、H+
B.该样品中Cu、O元素的质量比为10:1
C.V=448
D.溶解样品时消耗H2SO4的物质的量为0.04 mol
【答案】D
【解析】解:A.由于氧化性Fe3+>Cu2+>H+ , 铁离子优先反应,由于滤液A中不含铜离子,且硫酸足量,滤液A中阳离子为:Fe2+、H+ , 故A错误;
B.由以上分析可知样品中含有3.2gCu元素,铁元素的物质的量为0.04mol,质量为0.04mol×56g/mol=2.24g,则氧元素的质量为5.92g﹣3.2g﹣2.24g=0.48g,则该样品中Cu、O元素的质量比为3.2:0.48,故B错误;
C.最后溶液中溶质为过量H2SO4和FeSO4 , 而铁元素物质的量为0.04mol,说明参加反应硫酸物质的量为0.04mol,含氢离子0.08mol,其中部分氢离子生成氢气,另外的H+和合金中的氧结合成水了,由于合金中氧物质的量 ![]() =0.03mol,它结合氢离子0.06mol,所以硫酸中有0.08﹣0.06=0.02molH+生成氢气,即生成0.01mol氢气,标况体积为224ml,故C错误;
=0.03mol,它结合氢离子0.06mol,所以硫酸中有0.08﹣0.06=0.02molH+生成氢气,即生成0.01mol氢气,标况体积为224ml,故C错误;
D.铁元素的物质的量为0.04mol,铁与过量稀硫酸反应生成硫酸亚铁,则反应消耗硫酸的物质的量为0.04mol,故D正确.
故选D.


科目:高中化学 来源: 题型:
【题目】下列关于元素周期表和元素性质的叙述正确的是
A.质子数相同的微粒之间一定互称同位素
B.I A族与ⅦA族元素间形成的化合物一定是离子化合物
C.同主族元素的简单阴离子半径越大,其单质氧化性越弱
D.同周期金属元素的化合价越高,其氢氧化物的碱性越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂的保存或使用正确的是( )
A. 金属锂保存在煤油中,使用前要用滤纸吸干煤油
B. 过氧化钠比氧化钠稳定,因此过氧化钠可露置在空气中
C. 称量NaOH固体时,应先在天平两个托盘上各放一张等质量的纸,左边纸上放NaOH,右边纸上放砝码
D. 做焰色反应实验时,透过蓝色钴玻璃,观察到火焰颜色为紫色,证明被检验物中一定有钾元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,硫氢化钾溶液里存在下列平衡:a.HS-+H2O![]() OH-+H2S b.HS-
OH-+H2S b.HS-![]() H++S2-
H++S2-
(1)平衡a是__________平衡;平衡b是________平衡。(填“电离”或“水解”)
(2)向KHS溶液中加入氢氧化钠固体时,c(S2-)将________(填“增大”“ 减小”或“不变”,下同);向KHS溶被中通入HCl时,c(HS-)将______________。
(3)向KHS溶液中加入硫酸铜溶被时,有黑色沉淀(CuS)产生,则平衡a_________(填“正向” “逆向”或“不”,下同)移动,平衡b___________移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生活中常用来固定房门的“门吸”,它由磁铁和金属块两部分组成。该金属块能被磁铁所吸引,是因为可能含有以下材料中的
A. 银 B. 铁 C. 铝 D. 锌
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是 ( ) ①Na、Na2O、Na2 O2②AlCl3、Al(OH)3、NaAlO2
③Fe、FeCl2、FeCl3④NaOH、Na2CO3、NaHCO3 . 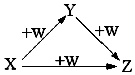
A.①②④
B.②④
C.①②③
D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.2 g 氦气所含有的原子数目是0.25 NA
B.常温常压下,0.5 mol Cl2所占有的体积约为11.2 L
C.标准状况下,0.9 mL水的质量约为0.9 g
D.0.5 mol/L Na2SO4 溶液中Na+ 的物质的量是1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com