
| A. | 高锰酸钾充分加热后的剩余固体、碘酒、空气都是混合物 | |
| B. | Na2O和NH3的水溶液均能导电,故均为电解质 | |
| C. | 氧化还原反应中非金属单质只作氧化剂 | |
| D. | 酸碱中和反应的实质是H+与OH-结合生成水,故酸碱中和反应都可用H++OH-═H2O表示 |
分析 A.不同物质组成的为混合物;
B.水溶液中或熔融状态下导电的化合物为电解质;
C.氧化还原反应中元素化合价降低做氧化剂;
D.强酸强碱中和反应可用H++OH-═H2O表示,弱酸弱碱反应不能写成氢离子和氢氧根离子.
解答 解:A.高锰酸钾充分加热后的剩余固体为二氧化锰和锰酸钾的混合物、碘酒是碘单质的酒精溶液、空气是不同气体组成都是混合物,故A正确;
B.Na2O和NH3的水溶液均能导电,但NH3不能电离,溶于水生成了电解质一水合氨,氨气属于非电解质,氧化钠熔融状态导电为电解质,故B错误;
C.氧化还原反应中非金属单质可以作氧化剂,也可以做还原剂,如氯气和水的反应中氯气即做氧化剂也做还原剂,故C错误;
D.弱酸弱碱中和反应,酸碱不能拆成离子,不能用H++OH-═H2O表示,故D错误;
故选A.
点评 本题考查了物质分类、电解质和非电解质概念、氧化还原反应实质、离子方程式书写等知识点,掌握基础是解题关键,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,32gO2含2NA个原子 | |
| B. | 标准状况下,11.2LH2O含有的原子数目为1.5NA | |
| C. | 1mol的Cl-含有NA个电子 | |
| D. | 0.5mol/L的NaCl溶液中Cl-的个数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
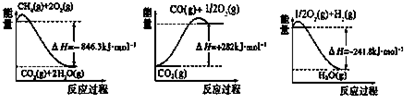
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol苯乙烯(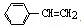 )中含有的C=C数为4NA )中含有的C=C数为4NA | |
| B. | 标准状况下,2.24L己烷含有的分子数为0.1NA | |
| C. | 1mol甲基含10NA个电子 | |
| D. | 某温度下,2.6g乙炔和苯的混合气体中所含碳原子数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| SO2 | O2 | SO2 | O2 | |||
| 1 | T1 | 4 | 2 | x | 0.8 | 6 |
| 2 | T2 | 4 | 2 | 0.4 | y | 9 |
| A. | x=1.6 | |
| B. | 实验 1 在前 6min 的反应速率 v(SO2)=0.2mol•L-1•min-1 | |
| C. | T1、T2的关系:T1>T2 | |
| D. | K1、K2的关系:K1>K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②③④ | B. | 只有③⑤ | C. | 只有①④⑥ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
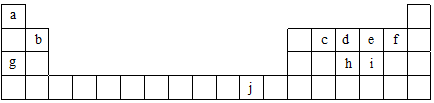
 .
. ,ci2与ce2比较,沸点较高的是CS2(写分子式).
,ci2与ce2比较,沸点较高的是CS2(写分子式).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
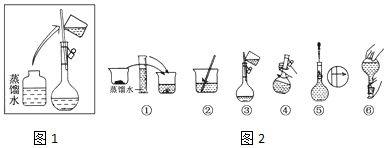
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com