
 CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011| 温度(K) | 500 | 600 | 700 | 800 |
| CO2转化率(%) | 60 | 43 | 28 | 15 |
 的值,K值______(填“增大”、“减小”或“不变”),对生产乙醇______(填“有利”或“不利”).
的值,K值______(填“增大”、“减小”或“不变”),对生产乙醇______(填“有利”或“不利”).
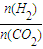 的值有利于平衡向正反应方向移动;
的值有利于平衡向正反应方向移动; ,
,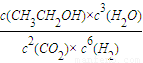 ;
;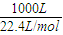 =44.6mol,
=44.6mol, ×44.6mol=22.3mol,
×44.6mol=22.3mol,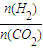 的值有利于平衡向正反应方向移动,故答案为:不变;有利;
的值有利于平衡向正反应方向移动,故答案为:不变;有利;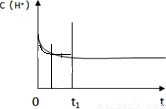 ;
;

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:阅读理解
 CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011
CH3CH2OH(g)+3H2O(g) 25℃时,K=2.95ⅹ1011| c(CH3CH2OH)×c3(H2O) |
| c2(CO2)×c6(H2) |
| c(CH3CH2OH)×c3(H2O) |
| c2(CO2)×c6(H2) |
| 温度(K) | 500 | 600 | 700 | 800 |
| CO2转化率(%) | 60 | 43 | 28 | 15 |
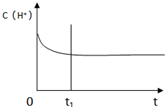
| n(H2) |
| n(CO2) |
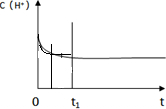

查看答案和解析>>
科目:高中化学 来源: 题型:
 Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.
Ⅰ、电解原理在化学工业中有广泛应用.图表示一个电解池,装有电解液c;A、B是两块电极板,通过导线与直流电源相连.查看答案和解析>>
科目:高中化学 来源: 题型:
①甲烷气体泄漏于大气中会造成怎样的环境问题?_________________________________。
②请你运用所学的物质结构知识解释“可燃冰”为何易融化放出气体?__________________。
(2)设计出燃料电池使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一。最近有人设计了一种燃料电池,一个电极通入空气,另一个电极通入液化石油气(以C4H10表示),电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-。
①已知该电池的负极反应为:C4H10+13O2--26e-![]() 4CO2+5H2O,则该电池的正极反应式为____________,电池工作时,固体电解质里的O2-向__________极移动。
4CO2+5H2O,则该电池的正极反应式为____________,电池工作时,固体电解质里的O2-向__________极移动。
②液化石油气燃料电池最大的障碍是氧化还原反应不完全而产生的____________(填写物质的名称)堵塞电极的气体通道。
(3)能源的紧缺在很大程度上制约了我国经济的发展,请你提出解决能源紧缺问题的两点建议:
①_________________________________________________________________,
②__________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)蕴藏在海底的“可燃冰”是在高压下形成的外观像冰的甲烷水合物固体,我国南海海底有极其丰富的“可燃冰”资源。将“可燃冰”从海底取出时易融化,释放出的甲烷气体将泄漏于大气中而产生严重的环境问题,这是目前开采“可燃冰”遇到的技术难题,请据此回答:
①甲烷气体泄漏于大气中会造成怎样的环境问题?答: ?? 。
②请你运用所学的物质结构知识解释“可燃冰”为何易融化放出气体?
答: ?? 。
(2)设计出燃料电池使液化石油气氧化直接产生电流是新世纪最富有挑战性的课题之一。最近有人设计了一种燃料电池,一个电极通入空气,另一个电极通入液化石油气(以C4H10表示),电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-。
①已知该电池的负极反应为:C4H10+13O2--26e- 4CO2+5H2O,则该电池的正极反应式为 ?? ,电池工作时,固体电解里的O2-向 极移动。
②液化石油气燃料电池最大的障碍是氧化还原不完全而产生的 ?? (填写物质的名称)堵塞电极的通气管道。
(3)能源的紧缺在很大程度上制约了我国的经济发展,请你提出解决能源紧缺问题的两点建议:① ?? ,
② ?? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com