
能从以下反应
①CaCO3+2HCl====CaCl2+CO2↑+H2O
![]() +CO2+H2O→
+CO2+H2O→![]() +NaHCO3
+NaHCO3
②2KMnO4+16HCl====2KCl+2MnCl2+5Cl2↑+8H2O
2KBr+Cl2====2KCl+Br2
推出的结论为( )
A.酸性:C6H5OH>HCl>H2CO3
B.酸性:HCl>H2CO3>C6H5OH
C.氧化性:KMnO4>Cl2>Br2
D.氧化性:Cl2>Br2>KMnO4
科目:高中化学 来源: 题型:
| HA | H2B | HC | ||
| Ka | Ka1 | Ka2 | Ka | |
| 数值 | 1.8×10-5 | 4.3×10-7 | 5.6×10-11 5.6×10-11 |
4.9×10-10 4.9×10-10 |
 (3)如图是某水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时的组成分数.
(3)如图是某水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时的组成分数.查看答案和解析>>
科目:高中化学 来源: 题型:
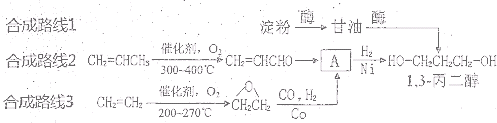
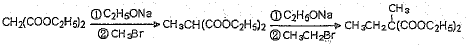
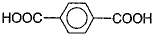 )为原料可以合成聚酯PTT,写出其化学方程式
)为原料可以合成聚酯PTT,写出其化学方程式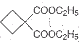 ,再转化为.
,再转化为.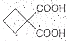 的同分异构体不可能属于
的同分异构体不可能属于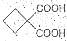 要合成,必须先合成哪些物质?(用合成该物质的化学方程式回答)
要合成,必须先合成哪些物质?(用合成该物质的化学方程式回答)查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省宁波市高三上学期期末考试化学试卷(解析版) 题型:填空题
(1)三种弱酸HA、H2B、HC,电离常数为1.8×10-5、5.6×10-11、4.9×10-10、4.3×10-7(数据顺序已打乱),已知三种酸和它们的盐之间能发生以下反应:
①HA+HB-(少量)=A-+H2B ②H2B(少量)+C-=HB-+HC
③HA(少量)+C-=A-+HC
若H2B的Ka1=4.3×10-7,则另二种酸对应的电离常数分别为(根据已知数据填
空):HA的Ka= ,HC的Ka= 。
(2)25 ℃时0.1 mol·L-1的H2R水溶液中,用氢氧化钠来调节溶液pH,得到含有H2R、
HR-、R2-三种微粒的溶液。当c(Na+)=c(R2-)+c(HR-)+c(H2R)时溶液的溶质
为 (填化学式)。
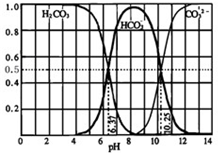
(3)下图是某水溶液在pH从0至14的范围内H2CO3、HCO3-、CO32-三种成分平衡时的组成分数。

①下列叙述正确的是 。
A.此图是1.0 mol·L-1碳酸钠溶液滴定1.0 mol·L-1 HCl溶液的滴定曲线
B.在pH分别为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-)
C.人体血液的pH约为7.4,则CO2在血液中多以HCO3-形式存在
D.若用CO2和NaOH反应制取NaHCO3,宜控制溶液的pH为7~9之间
②已知Ksp(CaCO3)=5.0×10-9,在10 mL 0.02 mol·L-1的Na2CO3溶液中,加入某浓度的盐酸,调节溶液的pH=10.25,此时溶液的体积恰好为100 mL,向该溶液中加入1 mL 1×10-4 mol·L-1的CaCl2溶液,问是否有沉淀生成? (填“是”或“否”)。
查看答案和解析>>
科目:高中化学 来源:下城区模拟 题型:填空题
| HA | H2B | HC | ||
| Ka | Ka1 | Ka2 | Ka | |
| 数值 | 1.8×10-5 | 4.3×10-7 | ______ | ______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com