
| A. | Al3+、NH4+、Cl-、SO42- | B. | Na+、Cl-、SO42-、HCO3- | ||
| C. | Na+、CH3COO-、NO3-、K+ | D. | K+、Na+、Cl-、SO42- |
分析 某溶液加入金属铝能放出氢气,为非氧化性酸或强碱溶液,根据离子之间不能结合生成沉淀、气体、水等,不能发生氧化还原反应等,则离子大量共存,以此来解答.
解答 解:某溶液加入金属铝能放出氢气,为非氧化性酸或强碱溶液,
A.碱溶液中不能大量存在Al3+、NH4+,故A不选;
B.酸、碱溶液中均不能大量存在HCO3-,故B不选;
C.酸溶液中不能大量存在CH3COO-,且Al、NO3-、H+发生氧化还原反应不生成氢气,故C不选;
D.酸、碱溶液中该组离子之间均不反应,可大量共存,故D选;
故选D.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,注意复分解反应及氧化还原反应的判断,题目难度不大.


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:实验题
 (1)已知H-H 键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.则N≡N键的键能是945.6kJ•mol-1
(1)已知H-H 键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.则N≡N键的键能是945.6kJ•mol-1查看答案和解析>>
科目:高中化学 来源: 题型:实验题
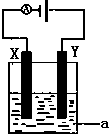
 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.请回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO+H2O═CO2+H2 | B. | 4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||
| C. | 2F2+2H2O═4HF+O2 | D. | 2Al+2NaOH+2H2O═2NaAlO2+3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.
(1)用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为环境修复研究的热点之一.Fe还原水体中NO3-的反应原理如图所示.| 化学键 | H-H | C-O | C-O | H-O | C-H |
| E/(KJ•mol-1) | 436 | 343 | 1075 | 465 | 413 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,2mol SO2与足量O2反应可得到2mol SO3 | |
| B. | 含4mol HCl的浓盐酸与足量的MnO2加热反应可制备1mol Cl2 | |
| C. | 10mL 18.0mol/L H2SO4与足量铜加热反应可制备0.09mol SO2 | |
| D. | 一定条件下,1mol N2与3mol H2反应可制备1.0 mol NH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na和H2O | B. | Na2O和H2O | ||
| C. | Ca(OH)2和Na2CO3溶液 | D. | Ca(OH)2和NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com