
【题目】明代《本草纲目》中与“烧酒”有关的条目:用浓酒和糟入甑,蒸令气上…其清如水,味极浓烈,盖酒露也”。下列说法正确的是( )
A.“烧酒”为纯净物
B.“酒露”为有刺激性气味的气体
C.“烧酒”的制作过程中没有物理变化
D.这里制作“烧酒”的方法是指蒸馏
 科学实验活动册系列答案
科学实验活动册系列答案科目:高中化学 来源: 题型:
【题目】某化学小组采用类似制乙酸乙酯的装置(如图1),以环己醇制备环己烯.
已知: ![]()
密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | ﹣103 | 83 | 难溶于水 |
(1)制备粗品将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.
①A中碎瓷片的作用是 , 导管B除了导气外还具有的作用是 .
②试管C置于冰水浴中的目的是 .
(2)制备精品①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环己烯在层(填“上”或“下”),分液后用(填选项字母)洗涤.
a.KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将环己烯按如图2装置蒸馏,冷却水从进入.蒸馏时要加入生石灰,目的是 .
③收集产品时,控制的温度应在左右,实验制得的环己烯精品质量低于理论产量,可能的原因是(填选项字母).
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是(填选项字母).a.用酸性高锰酸钾溶液 b.用金属钠 c.用溴水 d.测定沸点.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列描述中,不正确的是( )
A. 14N与15N具有相同的质子数 B. 18O和17O具有相同的电子数
C. 18O与19F具有相同的中子数 D. 12C与13C具有相同的质量数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)
研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。
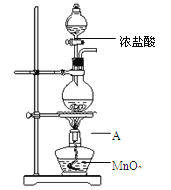
(1)仪器A的名称为 ;A中反应的离子方程式为 。
(2)甲同学将A中产生的气体通入下列溶液:
实验序号 | 试剂 | 现象 |
a | 紫色石蕊溶液 |
|
b | AgNO3溶液 | 出现白色沉淀 |
①实验a中的现象为 。
②不能证明产生的气体中含有HCl的实验是 (填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因: 。
(4)已知:2S2O32- + I2 === S4O62- + 2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl2。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 molL-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 molL-1 AgNO3溶液滴定所得溶液中的Cl-。
X中的HClO不会影响I的测定结果,原因是 。
由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 molL-1 AgNO3溶液的体积应大于 mL(用含V的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)(Ⅰ)已知在448℃时,反应H2(g)+I2(g)2HI(g)的平衡常数 K1为49,则该温度下反应2HI(g)H2(g)+I2(g)的平衡常数K2为![]() ;反应
;反应 ![]() H2(g)+
H2(g)+ ![]() I2(g)HI(g)的平衡常数K3为 .
I2(g)HI(g)的平衡常数K3为 .
(2)(Ⅱ)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
①该反应的化学平衡常数表达式为K= .
②该反应为反应(填“吸热”或“放热”).
③能判断该反应达到化学平衡状态的依据是 .
A.容器中压强不变 B.混合气体中c(CO)不变 C.v(H2)正=v(H2O)逆 D.c(CO2)=c(CO)
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2mol/L,c(H2)为1.5mol/L,c(CO)为1mol/L,c(H2O)为3mol/L,则下一时刻,反应向(填“正向”或“逆向”)进行.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学学习中要注重对过程的分析,按要求回答下列问题:
(1)向石蕊试液中通入氯气,观察到的现象是________________________,用化学方程式进行分析________________________________;若将氯水久置,将会有气泡冒出,用化学方程式进行分析_______________________________
(2)将一小块钠投入到盛FeCl3的溶液中,观察到的现象是__________________,用化学方程式进行分析________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸碱中和反应的本质是:H+ + OH- = H2O,下列物质间的反应可以用上述离子方程式表示的是( )
A. 氢氧化铁和稀盐酸反应 B. Ba(OH)2溶液滴入稀硫酸中
C. 澄清石灰水和稀硝酸反应 D. 氨水与盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com