
下列各表为周期表的一部分(表中为原子序数),其中正确的是( )
| | 2 | | | 2 | 3 | 4 | | | 6 | | | | 6 | 7 |
| 11 | | | | 11 | | 11 | 12 | 13 | | 14 | | |||
| 19 | | | | 19 | | | 24 | | 31 | 32 | |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
甲、乙、丙、丁、X是由短周期元素组成的纯净物,其中X为单质。上述物质转化关 系如下图所示(某些产物略去)。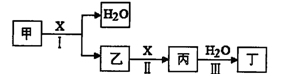
请回答下列问题:
(1)若丁是一元强酸,甲→丁是工业生产丁的主要途径。
①写出反应I的化学方程式: 。
②常温下,1 mol丙发生反应III放出46kJ热量,该反应的热化学方程式为: 。
③在常温下,向V1L pH= 11的甲溶液中加入V2L pH=3的盐酸,若反应后溶液的pH<7,则V1和V2的关系为V1 V2(选填“>”、“<”或“=”),所得溶液中各种离子的浓度由大到小的顺序可能是: (写一种即可)。
(2)若丁是二元弱酸,丙是温室气体。
在容积为2L的容积固定的密闭容器中,将乙(g)和H2O(g)按下表用量分别进行反应:乙(g)+H2O(g)  丙(g) + H2(g),得到如下数据:
丙(g) + H2(g),得到如下数据: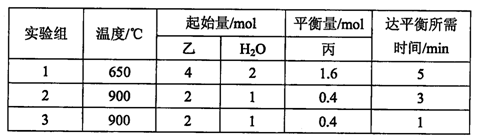
①该反应的正反应为 (填“吸热”或“放热”)反应。
②900℃时,上述反应按如下起始量分别加入该容器:
则此时反应的v(正) v(逆)(填“>”、“<”或“=”)。
③实验3跟实验2相比,改变的条件可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列结论正确的是 ( )
①粒子半径:K>Cl>S ②氢化物稳定性:HF>H2S>PH3;
③离子还原性:S2->Cl->Br->I- ④单质氧化性:Cl2>S>Si;
⑤酸性:H2SO4>HClO ⑥碱性强弱:KOH>NaOH>Mg(OH)2
| A.①④⑤ | B.③⑥ | C.②④⑤⑥ | D.①③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的3倍,下列说法正确的是
| A.X的氢化物溶于水生成弱酸 | B.Z的氢化物的水溶液在空气中存放不易变质 |
| C.Y与X可生成Y3X2型化合物 | D.Z的单质在氧气中燃烧可以生成两种酸性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( ) 
| A.原子半径:Z>Y>X |
| B.气态氢化物的稳定性:W > R |
| C.WX3和水反应形成的化合物是离子化合物 |
| D.Y和Z两者最高价氧化物对应的水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列各组顺序的排列不正确的是( )
| A.原子半径:Na > Mg > Al > H | B.热稳定性: HCl < H2S < PH3 |
| C.酸性强弱:H2SiO3< H2CO3< H3PO4 | D.氧化性:K+ < Na+ < Mg2+ < Al3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com