

 .
. 分析 小球表示碳原子,小棍表示化学键,每个C形成4个键,由图可知,
(1)只有A、C中含碳碳单键,且为饱和链状结构;
(2)分子式相同,结构不同的有机物互为同分异构体;
(3)H中含C个C、8个H,且为环状结构.
解答 解:小球表示碳原子,小棍表示化学键,每个C形成4个键,由图可知,
(1)只有A、C中含碳碳单键,且为饱和链状结构,则属于烷烃的是A、C,故答案为:A、C;
(2)A与C、B与EFH、D与G的分子式相同,结构不同,互为同分异构体,
故答案为:C;EFH; G;
(3)H中含C个C、8个H,且为环状结构,H的结构简式为 ,
,
故答案为: .
.
点评 本题考查有机物的结构及同分异构体的判断,为高频考点,把握球棍模型及有机物的结构为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 乙烯容易与溴的四氯化碳溶液发生反应,且1mol乙烯完全加成消耗1mol溴单质,证明乙烯分子里含有一个碳碳双键 | |
| B. | 苯分子的结构中存在碳碳单键和碳碳双键交替出现的结构 | |
| C. | 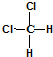 和 和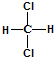 属于同一种物质,不能用来解释甲烷是一种正四面体结构 属于同一种物质,不能用来解释甲烷是一种正四面体结构 | |
| D. | 1mol CH3CH2OH与Na完全反应只生成0.5mol H2,不能说明乙醇分子中有一个氢原子与其它氢原子不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 如图表示A、B、C、D、E五种物质的相互转化关系,其中A为淡黄色固体,C为金属单质,D为最常用的调味品.
如图表示A、B、C、D、E五种物质的相互转化关系,其中A为淡黄色固体,C为金属单质,D为最常用的调味品.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
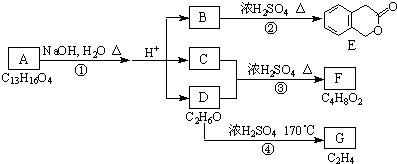
 .反应①的反应类型是水解反应.
.反应①的反应类型是水解反应. .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
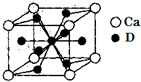 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 标准状况下,33.6 L氟化氢中含有氟原子的数目为1.5NA | |
| C. | 常温常压下,7.0 g乙烯与丙烯的混合物中含有氢原子的数目为NA | |
| D. | 某密闭容器盛有0.1 mol N2和0.3 mol H2,在一定条件下充分反应,转移电子的数目为0.6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 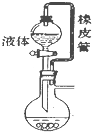 橡皮管能使液体顺利流下 | B. | 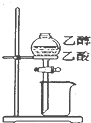 分离乙醇和乙酸 | ||
| C. | 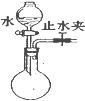 检查装置气密性 | D. | 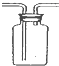 收集氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
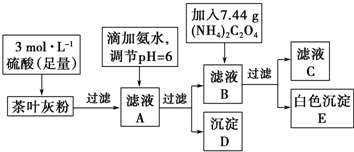
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com