
| A. | 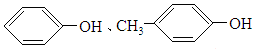 | B. | 甲苯和甘油(丙三醇) | ||
| C. | CH4、C2H4O2 | D. | C3H4、C3H6O |
分析 令烃及烃的含氧衍生物组成通式为CxHyOz,总物质的量一定时,以任意比混合,有机物完全燃烧消耗氧气的物质的量和生成水的物质的量不变,则化学式中的氢原子个数相同,每摩尔有机物耗氧量(x+$\frac{y}{4}$-$\frac{z}{2}$)mol相同即符合题意.
解答 解:A.分子式分别为C6H6O、C7H8O,H原子数不同,故当物质的量之和不变时,生成水的量随着两者的比例的不同而改变,故A错误;
B.分子式分别为C7H8,C3H8O3,1molC7H8燃烧(7+$\frac{8}{4}$)mol=9mol氧气,而1molC3H8O3燃烧消耗(3+$\frac{8}{4}$-$\frac{3}{2}$)=$\frac{7}{2}$mol氧气,故当物质的量之和不变时,混合物消耗的氧气的量随着两者的比例的不同而改变,故B错误;
C.1molCH4消耗2mol氧气,1molC2H4O2消耗2mol氧气,且两者中均含4个氢原子,故当两者的物质的量之和不变时,完全燃烧时消耗氧气和生成的水的物质的量也不变,故C正确;
D.C3H4和C3H6O的氢原子数不同,故当两者物质的量之和不变时,生成水的量随着两者的比例的不同而改变,故D错误;
故选C.
点评 本题考查有机物的燃烧计算,为高频考点,侧重考查学生的分析、计算能力的考查,掌握利用燃烧通式法进行的分析解答,本题中学生容易按照总质量一定来解答而出错.


科目:高中化学 来源: 题型:选择题
| A. | 其一氯代物可能只有一种 | |
| B. | 其分子中的共面原子最多6个 | |
| C. | 可用催化加氢反应除去C4H10中的C4H8 | |
| D. | 等质量的CH4和C4H8分别在氧气中完全燃烧,耗氧量CH4少于C4H8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蛋白质、炭黑、多糖、无机盐 | B. | 塑料、煤炭、多糖、无机盐 | ||
| C. | 多糖、炭黑、蛋白质、无机盐 | D. | 蛋白质、煤炭、多糖、有机玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
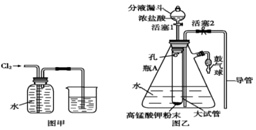 氯水是实验室常需临时配制的一种试剂,图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀的、可用于向瓶中鼓入空气的仪器).
氯水是实验室常需临时配制的一种试剂,图甲所示的是实验室配制氯水时的一种常用装置,图乙是某化学实验小组自行设计的一种配制氯水的装置(图中的鼓气球是一种具有气体单向阀的、可用于向瓶中鼓入空气的仪器).查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
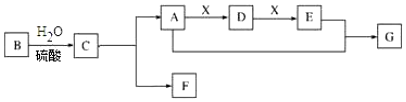
查看答案和解析>>
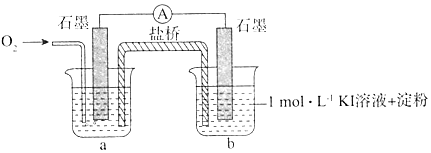
科目:高中化学 来源: 题型:实验题
| 装置 | 烧杯中的液体 | 现象(5分钟后) |
 | ①2mL1mol/LKl溶液+5滴淀粉 | 无明显变化 |
| ②2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L HCl | 溶液变蓝 | |
| ③2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L KCl | 无明显变化 | |
| ④2mL1mol/LKl溶液+5滴淀粉+2mL0.2mol/L CH3COOH | 溶液变蓝,颜色较②浅 |
| 烧杯中的液体 | 现象(5小时后) |
| ⑤2mLpH=8.5混有KOH的1mol/L KI溶液+5滴淀粉 | 溶液才略变蓝 |
| ⑥2mLpH=10混有KOH的1mol/L KI溶液+5滴淀粉 | 无明显变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 奶精能使溴水和酸性KMnO4溶液褪色,其原理相同 | |
| B. | 氢化植物油在稀H2SO4和NaOH溶液中发生水解,所得产物相同 | |
| C. | 白砂糖在人体内水解转化为果糖而被人体吸收 | |
| D. | 奶粉可作为人体所需的一种营养物质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com