
13C-NMR(核磁共振)可用于含碳化合物的结构分析14N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关13C、15N叙述正确的是( )
A.13C与15N具有相同的中子数 B.13C与C60是同一种物质
C.15N与14N互为同位素 D.15N的核外电子数与中子数相同
科目:高中化学 来源: 题型:
在一定条件下,把一定量NH3充入容积固定的密闭容器中,发生反应2NH3 (g)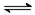 3H2(g)+N2(g)。达到平衡时,如果保持温度不变,增加N2的浓度。下列说法正确的是
3H2(g)+N2(g)。达到平衡时,如果保持温度不变,增加N2的浓度。下列说法正确的是
A.平衡向正反应方向移动 B.化学平衡常数不变
C.化学平衡常数增大 D.化学平衡常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能达到目的的是( )
A.用CCl4萃取碘水中的碘
B.将足量盐酸加入混有少量CaCO3杂质的Na2SO4中可除去杂质
C.将混有少量HCl的Cl2通入NaOH溶液中除去HCl
D.将Fe(OH)3固体加入沸水中制备Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
以铜为电极,a mol/L的硫酸铜溶液作电解液,对含有铁、锌、银的粗铜进行电解精炼,下列有关说法中正确的是( )
①粗铜应与电源的负极相连
②当有1 mol精铜析出时,就有2NA个电子通过电解质溶液
③阴极上的反应只有:Cu2++2e-===Cu
④电解结束时,c(CuSO4)<a mol/L
⑤杂质银以Ag2SO4形式沉入电解池形成“阳极泥”
A.②③ B.③④
C.①②④⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列实验装置进行相应实验,能达到实验目的的是( )

图1 图2 图3 图4
A.用图1 所示装置除去Cl2中含有的少量HCl
B.用图2 所示装置蒸发结晶提纯后的粗盐溶液,得NaCl晶体
C.用图3 所示装置制取少量纯净的CO2气体
D.用图4 所示装置分离用苯萃取碘水后已分层的有机层和水层
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
① CH4 (g)+4NO2 (g)=4NO (g) +CO2 (g)+2H2O (g) △H=-574 kJ·mol-1
② CH4 (g)+4NO (g)=2N2 (g)+CO2 (g)+2H2O (g) △H=-1160 kJ·mol-1。
下列选项正确的是( )
A.CH4 (g)+2NO2 (g)= N2 (g)+CO2 (g)+2H2O (l) △H=-867 kJ·mol-1
B.若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ
C.1molCH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子为3.2 mol
D.若用4.48L CH4还原NO2至N2,整个过程中转移的电子为3.2 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl = Na2Mn5O10+2AgCl,下列“水” 电池在海水中放电时的有关说法正确的是( )
A. 正极反应式:Ag+Cl--e-=AgCl
B. 每生成1 mol Na2Mn5O10转移2 mol电子
C. Na+不断向“水”电池的负极移动 D. AgCl是还原产物
查看答案和解析>>
科目:高中化学 来源: 题型:
三氯化磷(PCl3)是一种重要的有机合成催化剂。实验室常用红磷与干燥的Cl2制取PCl3,装置如下图所示。

已知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇O2会生成POCl3(三氯氧磷), POCl3溶于PCl3,PCl3遇水会强烈水解生成H3PO3和HCl。PCl3、POCl3的熔沸点见下表。
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
请回答:
(1)写出A中反应的离子方程式 。
(2)B装置中所盛试剂是 ;E中烧杯内冷水的作用是 。
(3)实验前玻璃管之间连接需要用到橡皮管,其连接方法是:先把 ,然后稍稍用力即可把玻璃管插入橡皮管中。
(4)检查装置气密性后,向D装置的曲颈瓶中加入红磷,打开K3通入干燥的CO2,一段时间后关闭K3,加热曲颈瓶至上部有黄色升华物出现时通入氯气,反应立即进行。其中通入干燥CO2的目的是 。
(5)实验制得的粗产品中常含有POCl3、PCl5等,加入红磷加热除去PCl5后,再通过 (填实验名称)即可得到较纯净的PCl3。
(6)实验后关闭K1,打开K2,将A、B中余氯通入300ml 1mol/L的NaOH溶液中。若NaOH恰好完全反应,则吸收氯气的物质的量为(假设反应生成了NaCl 、 NaClO 和 NaClO3 等钠盐) mol,反应中转移电子的物质的量(n)的范围是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L恒容密闭容器中充入2 mol X和lmol Y发生反应: , 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
, 反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
A.升高温度,平衡常数增大
B.W点X的正反应速率等于M点X的正反应速率
C.Q点时,Y的转化率最大
D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com