
分析 AgNO3是强酸弱碱盐,银离子水解导致溶液呈酸性,常温下pH<7,为防止AgNO3水解,所以配制AgNO3溶液时将AgNO3先溶于较浓的硝酸中,然后稀释,据此分析解答.
解答 解:AgNO3是强酸弱碱盐,银离子水解方程式为Ag++H2O?AgOH+H+,水解后溶液中c(H+)>c(OH-),所以溶液呈酸性,为防止AgNO3水解,应该向溶液中加入少量酸,所以配制AgNO3溶液时将AgNO3先溶于较浓的硝酸中,然后稀释,抑制银离子水解,
故答案为:抑制.
点评 本题考查盐类水解,根据盐类水解特点“谁强谁显性、谁弱谁水解、强强显中性”确定溶液酸碱性,会正确书写水解方程式,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
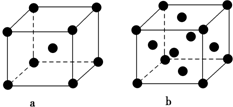
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
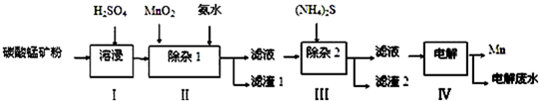
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该物质一定是钠的化合物 | B. | 该物质一定是金属钠 | ||
| C. | 该物质一定含钠元素 | D. | 可确定该物质中不含钾元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
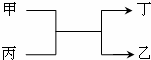 甲、乙为短周期同一主族元素的单质,丙、丁为氧化物,它们存在如图转化关系,下列各组的甲和乙一定符合的是( )
甲、乙为短周期同一主族元素的单质,丙、丁为氧化物,它们存在如图转化关系,下列各组的甲和乙一定符合的是( )| A. | 钠和氢 | B. | 氧和硫 | C. | 碳和硅 | D. | 氟和氯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
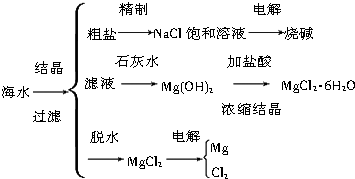
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com