
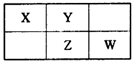
| A.元素Z位于周期表中第二周期,VA族 |
| B.W元素最高价氧化物的水化物酸性是同周期最强的 |
| C.这些元素中,Y的氢化物水溶液碱性最强 |
| D.四种元素中原子半径最大的为W |
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案科目:高中化学 来源:不详 题型:单选题
| A.还原性:Fe2+>I—>Br—>Cl— |
| B.氧化性:Fe3+ > Cu2+ >Zn2+ |
| C.酸性:H2SO4>CH3COOH> H2CO3>HClO |
| D.常温下跟钠反应的剧烈程度: 乙酸> 水>乙醇 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 性质 | A | B | C | D | E | F | G | H | I | J |
| 原子半径(10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | — | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | — | -2 | — | -4 | -3 | -1 | — | -3 | -4 |
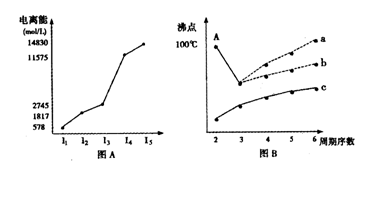
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.16O2与18O2互为同分异构体 |
| B.16O与18O核外电子排布方式不同 |
| C.通过化学变化可以实现18O与16O间的相互转化 |
| D.标准状况下,1.12 L16O2和1.12 L18O2均含0.1NA个氧原子 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| | B | C | D | |
| A | | E | ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
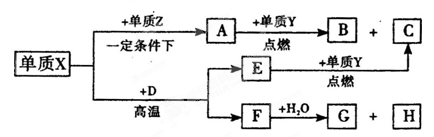
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
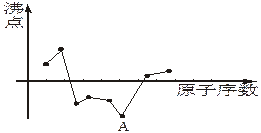
| A.C | B.Na | C.Ne | D.N |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
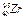 。专家表示,这些放射物质来自于核燃料棒。锆被发现了,说明堆心已经彻底熔毁;这不是几年就能解决的问题,最坏的情况发生了。日本前景堪忧!下列关于
。专家表示,这些放射物质来自于核燃料棒。锆被发现了,说明堆心已经彻底熔毁;这不是几年就能解决的问题,最坏的情况发生了。日本前景堪忧!下列关于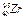 的说法正确的是
的说法正确的是A.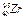 和 和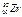 两原子的核外电子总数相等 两原子的核外电子总数相等 | B.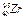 的中子数和电子数之差为55 的中子数和电子数之差为55 |
C.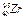 和 和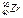 是同种核素 是同种核素 | D.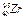 属于非金属元素 属于非金属元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com