
【题目】Lv(中文名“鉝”,lì)是元素周期表第116号元素。Lv原子的最外层电子数是6,下列说法中,不正确的是( )
A. Lv位于周期表第七周期第ⅥA族 B. ![]() Lv的原子核内的中子数比核外电子数少
Lv的原子核内的中子数比核外电子数少
C. 鉝的常见化合价可能有+6、+4 D. ![]() Lv、
Lv、![]() Lv、
Lv、![]() Lv互为同位素
Lv互为同位素
科目:高中化学 来源: 题型:
【题目】下列关于能量转化的认识中不正确的是( )
A. 镁在空气中燃烧时,化学能不只转化为热能
B. H2→H+H的变化需要吸收能量
C. 凡需要持续加热才能发生的化学反应都是吸热反应
D. 原电池工作时,化学能全部转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )
A.每生成2分子AB吸收b kJ热量
B.该反应热△H=+(a﹣b)kJmol﹣1
C.该反应中反应物的总能量高于生成物的总能量
D.断裂1 mol A﹣A和1 mol B﹣B键,放出a kJ能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲为恒压容器、乙为恒容容器.相同条件下充入等物质的量的NO2气体,且起始时体积相同.发生反应:2NO2(g)N2O4 (g)△H<0.一段时间后相继达到平衡状态.下列说法中正确的是( )
A.平衡时NO2体积分数:甲<乙
B.达到平衡所需时间,甲与乙相等
C.该反应的平衡常数表达式K=c(N2O4)/c(NO2)
D.若两容器内气体的压强保持不变,均说明反应已达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚铜的化合物经常具有令人惊奇的化学性质,常见的有CuH、CuCl等。
已知:CuCl熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,难溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为CuCl(白色,s)+3HCl(aq)![]() H3CuCl4(黄色,aq)。经常有两种方法制CuCl:
H3CuCl4(黄色,aq)。经常有两种方法制CuCl:
方法1:次磷酸H3PO2是一种强还原剂,将它加入CuSO4水溶液,加热到40~50℃,析出一种红棕色的难溶物CuH。待CuH生成后将A装置产生的HCl气体通入,可产生CuCl。

(1)写出H3PO2与CuSO4水溶液反应的化学方程式____________________。
(2)A装置中分液漏斗与圆底烧瓶中的物质依次为_________________________。
(3)刚开始通HCl气体时B装置中反应的化学方程式为______________________________。
(4)请描述从开始通HCl气体到通大量HCl气体过程中B装置中的观象_______________。
方法2:实验室用也可用如图所示装置制取CuCl,反应原理为:2Cu2++SO2+8Cl-+2H2O=2CuCl43-+SO42-+4H+
CuCl43-(aq)![]() CuCl(s)+3C1-(aq)
CuCl(s)+3C1-(aq)
装置B中反应结束后,取出混合物进行一系列操作可得到CuCl晶体。
(5)①在反应过程中SO2要过量通入的原因是______________________。
②欲提纯某混有铜粉的CuCl晶体,请简述实验方案:___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的量浓度相同的NaCl MgCl2 AlCl3三种溶液,当溶液的体积比为1:1:1时,三种溶液中Cl﹣的物质的量之比为( )
A.1:1:1
B.1:2:3
C.3:2:1
D.3:4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】作为工业生产的催化剂和制备纳米MgO的材料,草酸镁(MgC2O4·2H2O)有着广阔的应用和发展前景。回答下列问题:
(1)MgC2O4·2H2O的制备

已知氯化镁、草酸铵、草酸镁在水中的溶解度如下表:
氯化镁 | 草酸铵 | 草酸镁 | |
20℃ | 54.6g | 4.45g | 微溶 |
70℃ | 61.0g | 22.4g | |
100℃ | 73.3g | 34.7g |
实验方法:(i)加热煮沸蒸馏水,取300mL冷却至70℃,加140g MgCl2·6H2O,此制MgCl2溶液;
(ii)按照图示装置装好药品,连接好装置;
(iii)在磁力加热搅拌的情况下,缓缓滴入饱和(NH4)2C2O4溶液,并水浴加热,直至不再产生白色沉淀为止;
(iv)分离沉淀、洗涤,得MgC2O4·2H2O晶体。
①装置中仪器甲的名称是_____,其冷水进水口为_____填“a”或“b”)。
②仪器乙中c部位的作用是____________________。
③检验产品洗涤干净的方法是________________。
(2)MgC2O4·2H2O分解产物的探究
利用下图所示装置探究MgC2O4·2H2O分解产物CO、CO2 等的性质。
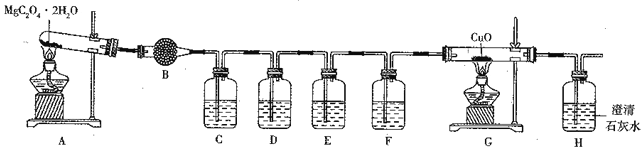
①A中发生反应的化学方程式为______________________。
②装置B中盛装的药品是_____,装置C的作用是______,装置D中的试剂是______,装置G中的现象是____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com