
【题目】在101 kPa时,1 g CH4完全燃烧生成CO2和液态H2O,放出55.64 kJ的热量。
(1)写出CH4燃烧热表示的热化学方程式。
(2)1000 L CH4(标准状况)燃烧后所产生的热量为多少?
【答案】
(1)CH4(g)+2O2 (g)=CO2(g)+2H2O(1)△H=-890kJ/mol;
(2)3.97×104kJ
【解析】
试题分析:(1)在101kPa时,1mol CH4 完全燃烧生成CO2和液态H2O,放出55.64 kJ×16= 890kJ的热量,根据燃烧热的概念,CH4的燃烧热△H=-890kJ/mol,CH4燃烧热的热化学方程式为CH4(g)+2O2 (g)=CO2(g)+2H2O(1)△H=-890kJ/mol,故答案为:CH4(g)+2O2 (g)=CO2(g)+2H2O(1)△H=-890kJ/mol;
(2)1000L CH4(标准状况)的物质的量是![]() mol,所以产生的热量为
mol,所以产生的热量为![]() mol×890kJ/mol=3.97×104kJ,故答案为:3.97×104kJ。
mol×890kJ/mol=3.97×104kJ,故答案为:3.97×104kJ。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】[实验化学]对氨基苯磺酸是制取染料和一些药物的重要中间体,可由苯胺磺化得到。
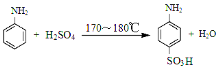
已知:100 mL水在20℃时可溶解对氨基苯磺酸1.08 g,在100℃时可溶解6.67 g。
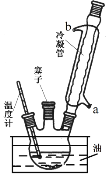
实验室可用苯胺、浓硫酸为原料,利用右图所示实验装置合成对氨基苯磺酸。实验步骤如下:步骤1:在一个250 mL三颈烧瓶中加入10 mL苯胺及几粒沸石,将三颈烧瓶放在冰水中冷却,小心地加入18 mL浓硫酸。在三颈烧瓶的两个瓶口上分别装冷凝管、温度计,另一个没有使用的瓶口用塞子塞紧。将三颈烧瓶置于油浴中缓慢加热至170~180℃,维持此温度2~2.5小时。
步骤2:将反应产物冷却至约50℃后,倒入盛有100 mL冷水的烧杯中,用玻璃棒不断搅拌,促使对氨基苯磺酸晶体析出。用该烧杯中的少量冷水将烧瓶内残留的产物冲洗到烧杯中,抽滤,用少量冷水洗涤,得到对氨基苯磺酸粗产品。
步骤3:将粗产品用沸水溶解,冷却结晶,抽滤,收集产品,晾干可得纯净的对氨基苯磺酸。
(1)实验装置中冷凝管由 处(填“a”或“b”)通入冷凝水。
(2)步骤1油浴加热的优点有 。
(3)步骤2中用玻璃棒不断搅拌可促使对氨基苯磺酸晶体析出的理由是 ,用少量冷水洗涤的目的是 。
(4)步骤2和3均进行抽滤操作,在抽滤完毕停止抽滤时,应注意先拆下连接泵和吸滤瓶的橡皮管,然后关闭水龙头,其目的是 。
(5)步骤3中若溶液颜色过深,可用 进行脱色处理。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用键能大小解释的事实是
A. 稀有气体化学性质很稳定 B. 硝酸易挥发,而硫酸难挥发
C. 氮气的化学性质比氧气稳定 D. 常温常压下,溴呈液态,碘呈固态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将6 mol H2和3 mol CO充入容积为0.5 L的密闭容器中,进行如下反应:
2H2(g)+CO(g)![]() CH3OH(g),6秒末时容器内压强为开始时的0.6倍。
CH3OH(g),6秒末时容器内压强为开始时的0.6倍。
试计算:(1)H2的反应速率是多少?(2)CO的转化率为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
A.达到化学平衡时4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增大容器容积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系:2v正(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化石墨烯(结构如图所示)是一种性能优异的新型碳材料。实验室制备氧化石墨烯的一种方法如下:

(1)将浓硫酸“冷却至0℃”可采用的方法是 。
(2) 步骤②采用100目鳞片状的石墨,其主要目的是 ;图示的“搅拌”方式为 。
(3)步骤③④中加NaNO3和KMnO4的作用是 。
(4)步骤⑧H2O2还原剩余的KMnO4反应的离子方程式为 ;检验洗涤已无SO42-的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学--选修物质结构与性质】
信息一:铬同镍、钴、铁等金属可以构成高温合金、电热合金、精密合金等,用于航空、宇航、电器及仪表等工业部门。
信息二:氯化铬酰(CrO2Cl2)是铬的一种化合物,常温下该化合物是暗红色液体,熔点为﹣96.5℃,沸点为117℃,能和丙酮(CH3COCH3)、四氯化碳、CS2等有机溶剂互溶。
(1)写出Fe(26号元素)原子的基态电子排布式为 。
(2)CH3COCH3分子中含有 个π键,含有 个δ键。
(3)固态氯化铬酰属于 晶体,丙酮中碳原子的杂化方式为 ,二硫化碳属于 (填极性”或“非极性”)分子。
(4)K[Cr(C2O4)2(H2O)2]也是铬的一种化合物,该化合物属于离子化合物,其中除含离子键、共价键外,还含有有 键。
(5)金属铬的晶胞如下图所示,一个晶胞中含有 个铬原子。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水热法制备Fe2O3纳米颗粒的反应是3Fe2++2S2O32-+O2+xOH-=Fe3O4+S4O62-+2H2O,关于该反应下列说法正确的是
A.H2O和S4O62-都是还原产物
B.1molFe2+参加反应时,转移2mol电子
C.Fe2+、S2O32-都是还原剂
D.x=2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com