
如图是元素周期表的一部分,下列对相关元素的叙述正确的是( )。
A.X元素的原子有二个电子层,处于周期表的第14纵行
B.Z的原子序数为31,单质常温下为液体
C.气态氢化物水溶液的酸性X<Z<Y
D.X的气态氢化物与Y的最高价氧化物的水化物能反应生成盐
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
被称为万能还原剂的NaBH4溶于水并和水反应:NaBH4+2H2O===NaBO2+4H2↑,下列说法中正确的是(NaBH4中H为-1价) ( )
A.NaBH4既是氧化剂又是还原剂
B.NaBH4是氧化剂,H2O是还原剂
C.硼元素被氧化,氢元素被还原
D.被氧化的元素与被还原的元素质量之比为1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏伽德罗常数的值,下列说法中正确的是( )。
A、84gNaHCO3晶体中含有NA个CO32-
B、9.2gNO2和N2O4的混合气体中含有的氮原子数为0.2NA
C、标准状况下,11.2L臭氧中含NA个氧原子
D.标准状况下,由Na2O2制得11.2 L O2,反应转移的电子数为0.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①将 通入酸性
通入酸性 溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________.
溶液中,溶液由紫色褪至无色。反应结束后,硫元素存在形式合理的是__________.
A.  B.
B.  C.
C.  D.
D. 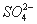
②亚硫酸钠中的硫呈+4价,它既有氧化性又有还原性,现在有试剂:溴水、H2S、稀硫酸。请选取合适的试剂证明Na2SO3具有还原性,并写出该反应的离子方程式为:_____________________________.
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由 、
、 、
、 、
、 组成。其中属于碱性氧化物的是______________________________。
组成。其中属于碱性氧化物的是______________________________。
②现取一份蛇纹石试样进行实验:
I. 先将其溶于过量的盐酸中、过滤,滤渣的主要成分是______________。
II. 再向滤液中加入 溶液至过量、过滤,滤渣中的主要成分是__________________。
溶液至过量、过滤,滤渣中的主要成分是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于浓硫酸和浓硝酸的叙述正确的是( )。
A.浓硫酸具有吸水性,因而能使蔗糖炭化
B.久置的浓硝酸会发黄,是因为HNO3不稳定,分解产生NO2溶于其中
C.常温下,浓硫酸和浓硝酸均可以与铜反应,放出气体
D.常温下可用铁制容器运输浓硫酸和浓硝酸,是因为它们与铁不反应
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应A (g)+ 3B(g) = 2C(g) + 2D(g),下列数据表示反应进行得最快的是( )。
A.v(A)=0.7mol/(L·s) B.v (B) =1.8mol/(L · s)
C.v (C)=1mol/(L·s) D.v (D) =1.6mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下的定容容器中,发生反应:2A(g)+B(s) C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
①混合气体的压强不变
②混合气体的密度不变
③C(g)的物质的量浓度不变
④容器内A、C、D三种气体的浓度之比为2:1:1
⑤单位时间内生成n molC,同时生成n mol D
⑥单位时间内生成n molD,同时生成2n mol A
A.①②⑤ B.①③⑥ C.②③⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两池电极材料都是铁棒与碳棒,请回答下列问题:
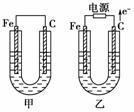
(1)若两池中均为CuSO4溶液,反应一段时间后:
①有红色物质析出的是甲池中的________棒,乙池中的________棒。
②乙池中阳极的电极反应式是_______________________________________________ _。
(2)若两池中均为饱和NaCl溶液:
①写出乙池中总反应的离子方程式__________________________________________。
②甲池中碳极上电极反应式是____________________,乙池中碳极上电极反应属于____________(填“氧化反应”或“还原反应”)。
③若乙池转移0.02 mol e-后停止实验,池中溶液体积是200 mL,则溶液混匀后的pH=________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com