
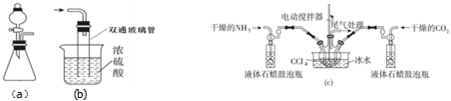
分析 (1)装置a是利用分液漏斗滴入液体溶解锥形瓶中的固体,利用溶解放热使氨水分解生成氨气;氨基甲酸铵在能溶于水和乙醇,而生成的氨基甲酸铵小晶体要悬浮在X中,据此选择;
(2)反应是放热反应降温平衡正向进行;
(3)液体石蜡鼓泡瓶的主要作用是控制反应进行程度,控制气体流速和原料气体的配比;
(4)生成的氨基甲酸铵小晶体悬浮在四氯化碳中,分离产品的实验方法利用过滤得到,氨基甲酸铵(NH2COONH4)是一种白色固体,易分解;
(5)依据反应过程中的产物分析,不能把污染性的气体排放到空气中,吸收易溶于水的气体需要放倒吸;
(6)碳酸氢铵的氨基甲酸铵样品中,使碳元素完全转化为碳酸钙,依据碳元素守恒和混合物质量计算物质的量分数.
解答 解:(1)把浓氨水滴入到固体氧化钙或氢氧化钠,在溶解过程中放热使浓氨水分解生成氨气,氨基甲酸铵在能溶于水和乙醇,而生成的氨基甲酸铵小晶体要悬浮在X中,所以X为四氯化碳,选B,
故答案为:浓氨水与生石灰(或氢氧化钠固体等);B;
(2)反应2NH3(g)+CO2(g)?NH2COONH4(s)+Q,是放热反应,降温平衡正向进行,温度升高;发生器用冰水冷却提高反应物质转化率,防止生成物温度过高分解,
故答案为:降低温度,提高反应物转化率(或降低温度,防止因反应放热造成产物分解);
(3)液体石蜡鼓泡瓶的作用是控制反应进行程度,控制气体流速和原料气体的配比,
故答案为:通过观察气泡,调节NH3与CO2通入比例;
(4)制备氨基甲酸铵的装置如图3所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中,分离产品的实验方法利用过滤得到,氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、不能加热烘干,应在真空40℃以下烘干,故选C,
故答案:过滤;C;
(5)双通玻璃管的作用是防止液体倒吸;浓硫酸起到吸收多余的氨气,同时防止空气中水蒸气进入反应器使氨基甲酸铵水解,
故答案为:防止倒吸;吸收多余氨气,防止空气中水蒸气进入反应器使氨基甲酸铵水解;
(6)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品0.7820g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.000g.物质的量为0.010mol,设样品中氨基甲酸铵物质的量为x,碳酸氢铵物质的量为y,依据碳元素守恒得到:x+y=0.01,根据总质量可得:78x+79y=0.7820,
解得:x=0.008mol、y=0.002mol,
则样品中氨基甲酸铵的物质的量分数为:$\frac{0.008mol}{0.01mol}$×100%=80%,
故答案为:80%.
点评 本题考查了物质制备实验的设计方法,涉及氨气的制备方法,氨基甲酸的制备实验装置分析判断、实验基本操作、混合物分离的实验设计、有关混合物的计算等知识,题目难度中等,明确实验目的、实验原理为解答关键,注意掌握制备实验方案的设计方法,试题培养了学生的分析、理解能力及化学实验能力.


 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案科目:高中化学 来源: 题型:解答题
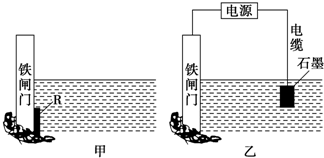 下面两个图都是金属防护的例子.
下面两个图都是金属防护的例子.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | Na2+ | Fe3+ | Cu2+ | Ca2+ | Mg2+ | Zn2- |
| 浓度/g•L-1 | 5.25 | 0.47 | 0.30 | 0.40 | 0.18 | 0.81 |
| 开始沉淀PH | 6.4 | 2.2 | 4.7 | / | 9.6 | 6.5 |
| 完全沉淀PH | 8.4 | 3.5 | 6.7 | / | 11.6 | 8.5 |
| 难溶物 | NiS | CuS | ZnS | |
| 溶度积常数 | 1.07×10-21 | 1.27×10-26 | 2.93×10-25 | |
| 难溶物 | CaF2 | MgF2 | ZnF2 | NiF2 |
| 溶度积常数 | 1.46×10-10 | 7.42×10-11 | 3.04×10-2 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
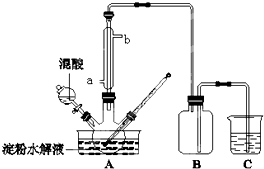 淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下:
淀粉水解的产物(C6H12O6)用硝酸氧化可以制备草酸,装置如图所示(加热、搅拌和仪器固定装置均已略去),实验过程如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有毒的 | B. | 单质 | C. | 氧化物 | D. | 金属或合金 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用KSCN溶于检验Fe2(SO4)3溶液中是否含有FeSO4 | |
| B. | 由同种元素组成的物质一定是纯净物 | |
| C. | 将钢闸门与电源正极相连,可防止其在海水中被腐蚀 | |
| D. | 浊液、胶体、溶液三种分散系的本质区别是分散质微粒直径的大小不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两极附近颜色无明显变化 | B. | 两极产生等量气体 | ||
| C. | 阳极附近的颜色变红 | D. | 阴极附近的颜色变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③⑤ | B. | ②③ | C. | 只有③ | D. | ①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com