
| A. | 溶液 | B. | 胶体 | C. | 悬浊液 | D. | 乳浊液 |
分析 雾属于胶体分散系.根据分散质粒子直径大小分类,把分散系分为:溶液、胶体、浊液.“纳米”是一个长度的单位,1 nm=10-9 m,溶液、浊液、胶体的本质区别就是分散质的微粒直径不同.
解答 解:雾霾,雾和霾的统称,霾的意思是灰霾(烟霞) 空气中的灰尘、硫酸、硝酸等造成视觉程障碍的叫霾.二氧化硫、氮氧化物和可吸入颗粒物这三项是雾霾主要组成,前两者为气态污染物,最后一项颗粒物才是加重雾霾天气污染的罪魁祸首.根据雾霾中分散质的微粒的直径小于等于2.5微米的污染物,可知:雾霾可能为胶体.
故选B.
点评 本题考查了分散系的组成及分类,题目难度不大,注意明确分散系的概念及分类方法,试题培养了学生灵活应用所学知识的能力.


 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是氧化剂,NaOH是还原剂 | |
| B. | 被氧化的Cl原子与被还原的Cl原子的个数比为1:5 | |
| C. | 氧化剂与还原剂的物质的量的比为1:2 | |
| D. | 每生成1mol的NaClO3转移6mol的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.08 | 0.08 |
| A. | 从反应开始直至60s和80s时,二氧化氮的平均反应速率是相等的 | |
| B. | 80s后将容器的体积缩小为1L,平衡向正反应方向移动,气体颜色变浅 | |
| C. | n1的范围是0.28<n1<0.33 | |
| D. | 升高温度,既能加快反应速率,也能提高N2O4的体积分数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
| A. | 反应至6min时,c(H2O2)=0.20mol/L | |
| B. | 反应至6min时,H2O2分解了40% | |
| C. | 0~6min的平均反应速率:v(H2O2)≈3.3×10-2mol/(L•min) | |
| D. | 6~10min的平均反应速率:v(H2O2)<3.3×10-2mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②③④ | C. | ②④⑤ | D. | ③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.8 g Na2O2与足量H2O反应,电子转移1.204×1023 NA个 | |
| B. | 16 g O2和O3的混合气体中,含O原子 NA个 | |
| C. | 1.12 L氯气中含有0.1 NA个氯原子 | |
| D. | 标准状况下,2.24 L水中含有0.1 NA个水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
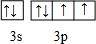 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com