
2H2O(g) ====2H2(g)+O2(g)ΘΜΠΛH=Q2 kJΓΛmol-1
CH4Θ®gΘ©+2O2(g) ====CO2(g)+2H2O(l)ΘΜΠΛH=-Q3 kJΓΛmol-1Θ§‘ρH2ΚΆCH4ΒΡ»Φ…’»»÷°±» «
A.![]() B.
B. ![]() C.
C.![]() D.
D.![]()

| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
H2(g)+![]() O 2(g)
O 2(g)![]() H2O(l)ΠΛH=-285.8 kJΓΛmol-1ΘΜC3H8(g)+5O2(g)
H2O(l)ΠΛH=-285.8 kJΓΛmol-1ΘΜC3H8(g)+5O2(g) ![]() 3CO2(g)+4H2O(l)
3CO2(g)+4H2O(l)
ΠΛH=-2 220.0 kJΓΛmol-1ΓΘ
(1) Β―ι≤βΒΟH2ΚΆC3H8ΒΡΜλΚœΤχΧεΙ≤5 molΘ§Άξ»Ϊ»Φ…’…ζ≥…“ΚΧ§Υ° ±Ζ≈»»6 264.5 kJΘ§ΜλΚœΤχΧε÷–H2ΚΆC3H8ΒΡΧεΜΐ±»______________________ΓΘ
(2)“―÷ΣΘΚH2O(l)![]() H2O(g) ΠΛH=+44.0 kJΓΛmol-1ΘΜ–¥≥ω±ϊΆι»Φ…’…ζ≥…CO2ΚΆΤχΧ§Υ°ΒΡ»»Μ·ΖΫ≥Χ Ϋ_____________________________________________________________________ΓΘ
H2O(g) ΠΛH=+44.0 kJΓΛmol-1ΘΜ–¥≥ω±ϊΆι»Φ…’…ζ≥…CO2ΚΆΤχΧ§Υ°ΒΡ»»Μ·ΖΫ≥Χ Ϋ_____________________________________________________________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2011-2012―ßΡξΚ”±± ΓΧΤ…Ϋ“Μ÷–ΗΏ“Μœ¬―ßΤΎΤΎ÷–ΩΦ ‘Μ·―ß ‘ΨμΘ®¥χΫβΈωΘ© Χβ–ΆΘΚΧνΩ’Χβ
“―÷Σ0.4 mol“ΚΧ§κ¬(N2H4)”κΙΐΝΩΒΡ“ΚΧ§ΥΪ―θΥ°Ζ¥”ΠΘ§…ζ≥…ΒΣΤχΚΆΥ°’τΤχΘ§Ζ≈≥ω256.65 kJΒΡ»»ΝΩΘ§ΗΟΖ¥”ΠΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ ΓΘ
”÷“―÷ΣΘΚH2O(l)=H2O(g)ΓΓΠΛH ΘΫΘΪ44 kJ/molΘ§‘ρ16 g“Κקꬔκ“ΚΧ§ΥΪ―θΥ°Ζ¥”Π…ζ≥…“ΚΧ§Υ° ±Ζ≈≥ωΒΡ»»ΝΩ « ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2013-2014―ßΡξΚΎΝζΫ≠ ΓΗΏΕΰ…œ―ßΤΎΤΎ÷–Μ·―ß ‘ΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚΧνΩ’Χβ
(8Ζ÷)(1)κ¬(N2H4) «ΖΔ…δΚΫΧλΖ…¥§≥Θ”ΟΒΡΗΏΡή»ΦΝœΓΘΫΪNH3ΚΆNaClOΑ¥“ΜΕ®Έο÷ ΒΡΝΩ±»ΜλΚœΖ¥”ΠΘ§…ζ≥…κ¬ΓΔNaClΚΆΥ°Θ§ΗΟΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ Ϋ «_____________________________ΓΘ
(2)‘ΎΜπΦΐΆΤΫχΤς÷–ΉΑ”–«ΩΜΙ‘≠ΦΝκ¬(N2H4)ΚΆ«Ω―θΜ·ΦΝΙΐ―θΜ·«βΘ§Β±ΥϋΟ«ΜλΚœ ±Θ§Φ¥≤ζ…ζ¥σΝΩΤχΧεΘ§≤ΔΖ≈≥ω¥σΝΩ»»ΓΘ“―÷ΣΘΚH2O(l) H2O(g) ΠΛH= +44 kJ/molΓΘ12.8 g“ΚקꬔκΉψΝΩΙΐ―θΜ·«βΖ¥”Π…ζ≥…ΒΣΤχΚΆΥ°’τΤχΘ§Ζ≈≥ω256.65 kJΒΡ»»ΝΩΓΘ
ΔΌ«κ–¥≥ω“ΚקꬔκΙΐ―θΜ·«βΖ¥”Π…ζ≥…“ΚΧ§Υ°ΒΡ»»Μ·―ßΖΫ≥Χ Ϋ______________________ΓΘ
ΔΎ‘ρ16 g “ΚקꬔκΉψΝΩΙΐ―θΜ·«βΖ¥”Π…ζ≥…“ΚΧ§Υ° ±Ζ≈≥ωΒΡ»»ΝΩ «___________________ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ2011-2012―ßΡξΫ≠Υ’ ΓΥ’÷–»ΐ –ΗΏ»ΐ5‘¬ΒΎΕΰ¥ΈΒς―–≤β ‘Μ·―ß ‘ΨμΘ®ΫβΈωΑφΘ© Χβ–ΆΘΚΧνΩ’Χβ
(14Ζ÷)““¥ΦΤϊ”Ά «±ΜΙψΖΚ Ι”ΟΒΡ–¬–Ά«εΫύ»ΦΝœΘ§ΙΛ“Β…ζ≤ζ““¥ΦΒΡ“Μ÷÷Ζ¥”Π‘≠άμΈΣΘΚ2CO(g)+4H2 (g)  CH3CH2OH(g)+H2O(g)
ΓςH=ΓΣ256.1kJΓΛmolΓΣ1ΓΘ
CH3CH2OH(g)+H2O(g)
ΓςH=ΓΣ256.1kJΓΛmolΓΣ1ΓΘ
“―÷ΣΘΚH2O(l)=H2O(g) ΓςH=+44kJΓΛmolΓΣ1
CO(g)+H2O(g) CO2(g)+H2(g)
ΓςH=ΓΣ41.2kJΓΛmolΓΣ1
CO2(g)+H2(g)
ΓςH=ΓΣ41.2kJΓΛmolΓΣ1
Δ≈“‘CO2(g)”κH2(g)ΈΣ‘≠Νœ“≤Ω…Κœ≥…““¥ΦΘ§Τδ»»Μ·―ßΖΫ≥Χ Ϋ»γœ¬ΘΚ
2CO2(g)+6H2(g)
 CH3CH2OH(g)+3H2O(l)
ΓςH= ΓΘ
CH3CH2OH(g)+3H2O(l)
ΓςH= ΓΘ
ΔΤCH4ΚΆH2O(g)‘Ύ¥ΏΜ·ΦΝ±μΟφΖΔ…ζΖ¥”ΠCH4+H2O CO+3H2Θ§ΗΟΖ¥”Π‘Ύ≤ΜΆ§Έ¬Ε»œ¬ΒΡΜ·―ßΤΫΚβ≥Θ ΐ»γœ¬±μΘΚ
CO+3H2Θ§ΗΟΖ¥”Π‘Ύ≤ΜΆ§Έ¬Ε»œ¬ΒΡΜ·―ßΤΫΚβ≥Θ ΐ»γœ¬±μΘΚ
|
Έ¬Ε»/Γφ |
800 |
1000 |
1200 |
1400 |
|
ΤΫΚβ≥Θ ΐ |
0.45 |
1.92 |
276.5 |
1771.5 |
ΔΌΗΟΖ¥”Π «_____Ζ¥”ΠΘ®ΧνΓΑΈϋ»»Γ±ΜρΓΑΖ≈»»Γ±Θ©ΘΜ
ΔΎTΓφ ±Θ§œρ1LΟή±’»ίΤς÷–ΆΕ»κ1molCH4ΚΆ1mol H2O(g)Θ§ΤΫΚβ ±c(CH4)=0.5molΓΛLΓΣ1Θ§ΗΟΈ¬Ε»œ¬Ζ¥”ΠCH4+H2O CO+3H2ΒΡΤΫΚβ≥Θ ΐK= ΓΘ
CO+3H2ΒΡΤΫΚβ≥Θ ΐK= ΓΘ
Δ«Τϊ≥Β Ι”Ο““¥ΦΤϊ”Ά≤Δ≤ΜΡήΦθ…ΌNOxΒΡ≈≈Ζ≈Θ§’β ΙNOxΒΡ”––ßœϊ≥ΐ≥…ΈΣΜΖ±ΘΝλ”ρΒΡ÷Ί“ΣΩΈΧβΓΘΡ≥―–ΨΩ–ΓΉι‘Ύ Β―ι ““‘Ag-ZSM-5 ΈΣ¥ΏΜ·ΦΝΘ§≤βΒΟNOΉΣΜ·ΈΣN2ΒΡΉΣΜ·¬ ΥφΈ¬Ε»±δΜ·«ιΩω»γΆΦΓΘ
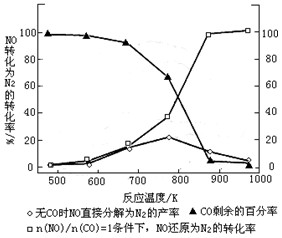
ΔΌ»τ≤Μ Ι”ΟCOΘ§Έ¬Ε»≥§Ιΐ775ΓφΘ§ΖΔœ÷NOΒΡΖ÷Ϋβ¬ ΫΒΒΆΘ§ΤδΩ…ΡήΒΡ‘≠“ρΈΣ ΘΜ‘Ύn(NO)/n(CO)=1ΒΡΧθΦΰœ¬Θ§”ΠΩΊ÷ΤΒΡΉνΦ―Έ¬Ε»‘Ύ Ήσ”“ΓΘ
ΔΎ”ΟCxHyΘ®ΧΰΘ©¥ΏΜ·ΜΙ‘≠NOx“≤Ω…œϊ≥ΐΒΣ―θΜ·ΈοΒΡΈέ»ΨΓΘ–¥≥ωCH4”κNO2ΖΔ…ζΖ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΘΚ ΓΘ
Δ»““¥Φ-Ω’Τχ»ΦΝœΒγ≥Ί÷– Ι”ΟΒΡΒγΫβ÷ «≤σ‘”ΝΥY2O3ΒΡZrO2ΨßΧεΘ§Υϋ‘ΎΗΏΈ¬œ¬Ρή¥ΪΒΦO2ΓΣάκΉ”ΓΘΗΟΒγ≥ΊΗΚΦΪΒΡΒγΦΪΖ¥”Π ΫΈΣ ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com