
【题目】用NA代表阿伏伽德罗常数的值,下列说法正确的是( )
A.将 100mL 0.1 molL﹣1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒数目为0.01NA
B.通常状况下,0.5 mol锌粒与足量盐酸反应产生11.2 L H2
C.常温常压下,2.4g金属镁变成镁离子时,失去的电子数为0.1NA
D.标准状况下,22.4L由N2和N2O组成的混合气体中,所含N原子的个数为2NA
科目:高中化学 来源: 题型:
【题目】2013年H7N9禽流感肆虐期间为了保证卫生环境,常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒,以抑制大规模传染病爆发.钠、镁及其化合物在工业中具有广泛的应用.回答下列问题:
(1)写出钠与水反应的化学方程式
(2)写出镁与二氧化碳反应的化学方程式
(3)漂白粉溶于水后,与空气中CO2发生反应,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为
(4)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质(填序号).
A.酸性
B.碱性
C.漂白性.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 摩尔是表示物质的数量单位
B. 1 mol氢的质量是2 g
C. O2的摩尔质量是32 g
D. 每摩尔粒子都含有阿伏加德罗常数个指定粒子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,a g气体A和b g气体B的体积相同,下列叙述正确的是( )
A.A和B的原子个数比是1:1
B.A和B的密度之比为b:a
C.A和B的摩尔质量比是a:b
D.A和B的分子数之比是b:a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物中
(1)属于芳香族化合物的是 ,
(2)属于芳香烃的是 ,
(3)属于苯的同系物的是 ,
(4)属于脂环烃的是 ,
(5)属于烃的衍生物的是(填序号) ① 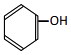 ②
②  ③
③ ![]() ④
④ ![]() ⑤
⑤  ⑥
⑥ 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空:
(1)已知16克A和20克B恰好完全反应生成0.05mol C和30克D,则C的摩尔质量为
(2)0.3mol氨气和0.4mol二氧化碳的质量(填“相等”或“不相等”,下同),所含原子数 .
(3)4g H2与22.4L(标准状况)CO2相比,所含分子数目较多的是 .
(4)3.01×1023个CO2分子中含mol氧原子,在标准状况下其体积为L,它与g H2O含有相同的氧原子数.
(5)写出下列物质的电离方程式:硫酸铵;氢氧化钡 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com