
某同学按如图所示的装置进行实验,A、B为常见金属,它们的硫酸盐可溶于水。当K闭合时,阴离子交换膜处的 从右向左移动。下列分析正确的是
从右向左移动。下列分析正确的是
A.A的金属活动性弱于B
B.Na+从y电极趋向x电极
C.Y电极附近溶液先变红
D.B的电极反应:
B
解析试题分析:根据题意知,该装置中右边装置为电解池,左边装置是原电池;A、当K闭合时,阴离子交换膜处SO42-从右向左移动,说明A为负极,B为正极,则A的金属活动性强于B,错误; B、右边装置中连接B的y极为阳极,连接A的x极为阴极,电解池工作时,Na+从y电极趋向x电极,正确; C、右边装置中y极上发生的电极反应式为2Cl--2e-=Cl2↑,x极上发生的电极反应式为2H++2e-=H2↑,由于氢离子放电而氢氧根离子不放电导致溶液呈碱性,X电极附近溶液先变红,错误;D、当K闭合时,阴离子交换膜处SO42一从右向左移动,说明A为负极,B为正极,B极上溶液中的金属阳离子得电子生成金属单质,电极反应式为B2++2eˉ═B,错误。
考点:考查原电池和电解池原理。


科目:高中化学 来源: 题型:单选题
有下图所示装置:
(1)装置A中b为 极,电极反应式为 ,a极反应式为 ;
(2)装置B中C为 极,电极反应式为 。
(3)当铁电极的质量变化为12.8g时,a极上消耗O2在标准状况下的体积为 L。
(4)若将装置B中的CuSO4溶液更换为100mL滴有酚酞的饱和NaCl溶液,电解一段时间后 极附近颜色变红,当装置A中消耗0.05mol氢气时,装置B中溶液的pH为 。
(5)若将装置B改为电解精炼铜,则粗铜作 极,另一极反应为 。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关物质的性质和该性质的应用均正确的是 ( )
| A.常温下浓硫酸与铝不发生反应,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.二氧化氯具有氧化性,可用于自来水的杀菌消毒 |
| D.铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是:
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是:
| A.放电时正极反应为:FeO42-+4H2O+3e-=Fe(OH)3+5OH- |
| B.充电时阴极反应为:Zn(OH)2+2e-=Zn+2OH- |
| C.放电时每转移3mol电子,正极有1mol K2FeO4被氧化 |
| D.充电时阳极附近溶液的pH减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
有关下图的说法正确的是( )
| A.构成原电池时溶液中SO42-移向Cu极 |
| B.构成原电池时Cu极反应为: Cu﹣2e-=Cu2+ |
| C.要使Fe极不被腐蚀,Cu片换Zn片或a接直流电源负极 |
| D.a和b分别接直流电源正、负极,Fe片上有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
发展混合动力车是实施节能减排的重要措施之一。汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态以节省能耗。混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)电解液。镍氢电池充放电原理总反应式为:H2+2NiOOH 2Ni(OH)2。下列有关混合动力车的判断正确的是:
2Ni(OH)2。下列有关混合动力车的判断正确的是: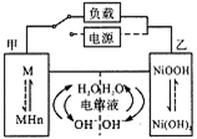
| A.在上坡或加速时,乙电极周围溶液的pH将减小 |
| B.在上坡或加速时,溶液中的K+向甲电极迁移 |
| C.在刹车和下坡时,乙电极增重 |
D.在刹车和下坡时,甲电极的电极反应式为:2H2O+2e- H2↑+2OH- H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列四种装置中,溶液的体积均为250 mL,开始时电解质溶液的浓度均为0.10mol/L,工作一段时间后,测得导线上均通过0.02 mol电子,若不考虑溶液体积的变化,则下列叙述正确的是
| A.工作一段时间后溶质的物质的量浓度①=②=③=④ |
| B.工作一段时间后溶液的pH:④>③=①>② |
| C.产生气体的总体积:④>②>①>③ |
| D.电极上析出的固体的质量:①>②>③>④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
热激活电池可用作火箭、导弹的工作电源。其基本结构如图所示,作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池的总反应方程式为:
PbSO4+2LiCl+Ca CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
CaCl2+Li2SO4+Pb。下列有关说法正确的是( )
A.正极反应式:Ca+2Cl--2e- CaCl2 CaCl2 |
| B.常温时,在正负极间接上电流表或检流计,指针不偏转 |
| C.放电过程中,Li+向负极移动 |
| D.每转移0.1 mol电子,理论上生成20.7 g Pb |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知氧化性:Au3+>Ag+>Cu2+>Pb2+>Cr3+>Zn2+>Ti2+。现有如图所示的电化学装置,下列叙述中正确的是
| A.若X为Ti,则Y极的电极反应式可能是Zn-2e-=Zn2+ |
| B.若X为Cr,则Y可以选Zn或Ti |
| C.若Y为Cu,则X极的电极反应式可能是Cr-3e-=Cr3+ |
| D.若Y为Pb,则Xn+(aq)中阴离子数会减少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com