
Ⅰ:(1)氢气被人们看作理想的绿色能源,己知氢气的热值是143 kJ·g-1.请写出氢气燃烧的热化学方程式________.
(2)1 mol N2(g)和1 mol O2(g)在一定条件下反应生成2 mol NO(g),吸收180 kJ的热量,已知断裂1 mol N2(g)中的N≡N和1 mol O2(g)中的O=O分别需要吸收946 kJ和498 kJ的能量,则1 mol NO分子中的化学键形成时可释放________kJ的能量.
Ⅱ:在一个U形管里盛有氯化铜溶液,并插入两块锌片作电极,如图所示:
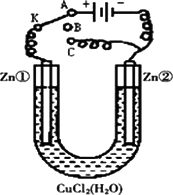
(1)如果把电键K接A,这一装置形成________装置,Zn①极是________极,其电极反应式是________.
(2)上述反应进行5 min后,转换电键K到C,这一装置形成________装置,Zn②极是________极,其电极反应式是________;
(3)上述装置进行2 min后,再转换电键K到B,在Zn②极上发生的腐蚀属于________,Zn①极发生的腐蚀主要属于________.
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:江西省上高二中2011-2012学年高一下学期第二次月考化学试题 题型:022
Ⅰ、一定温度下,在容积为V L的密闭容器中进行反应:aN(g)![]() bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中![]() =________
=________
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:________
(3)平衡时,N的转化率为________.
(4)下列叙述中能说明上述反应达到平衡状态的是________
A.反应中M与N的物质的量之比为1∶1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
Ⅱ、(1)氢气被人们看作理想的绿色能源,己知氢气的热值是143 kJ·g-1.则燃烧1 mol H2放出的热量为________kJ.
(2)1 mol N2(g)和1 mol O2(g)在一定条件下反应生成2 mol NO(g),吸收180 kJ的热量,已知断裂1 mol N2(g)中的N≡N和1 mol O2(g)中的O=O分别需要吸收946 kJ和498 kJ的能量,则1 mol NO分子中的化学键形成时可释放________kJ的能量.
查看答案和解析>>
科目:高中化学 来源:2011-2012学年江西省上高二中高一下学期第二次月考化学试卷(带解析) 题型:填空题
(12分)I、一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:
(1)此反应的化学方程式中 =__________
=__________
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:____________
(3)平衡时,N的转化率为 。
(4)下列叙述中能说明上述反应达到平衡状态的是
| A.反应中M与N的物质的量之比为1︰1 |
| B.混合气体的总质量不随时间的变化而变化 |
| C.混合气体的总物质的量不随时间的变化而变化 |
| D.单位时间内每消耗a mol N,同时生成b mol M |
查看答案和解析>>
科目:高中化学 来源:2014届江西省高一下学期第二次月考化学试卷(解析版) 题型:填空题
(12分)I、一定温度下,在容积为V L的密闭容器中进行反应:aN(g) bM(g),M、N的物质的量随时间的变化曲线如图所示:
bM(g),M、N的物质的量随时间的变化曲线如图所示:

(1)此反应的化学方程式中 =__________
=__________
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:____________
(3)平衡时,N的转化率为 。
(4)下列叙述中能说明上述反应达到平衡状态的是
A.反应中M与N的物质的量之比为1︰1
B.混合气体的总质量不随时间的变化而变化
C.混合气体的总物质的量不随时间的变化而变化
D.单位时间内每消耗a mol N,同时生成b mol M
E.混合气体的压强不随时间的变化而变化
F.N的质量分数在混合气体中保持不变
II、(1)氢气被人们看作理想的绿色能源,己知氢气的热值是143kJ·g-1。则燃烧1molH2放出的热量为 kJ。
(2)1molN2(g)和1molO2(g)在一定条件下反应生成2molNO(g),吸收180kJ的热量,已知断裂1molN2(g)中的N≡N和1molO2(g)中的O=O分别需要吸收946kJ和498kJ的能量,则1molNO分子中的化学键形成时可释放_______kJ的能量。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com