
【题目】25℃时,体积均为20 mL、浓度均为0.1mol/L的两种酸HX、HY分别与0.1mol/L的NaOH溶液反应,所加NaOH溶液体积与反应后溶液的pH的关系如图所示。下列叙述正确的是

A. 加入10 mL NaOH溶液时,a点c(X-)<b点c(Y-)
B. b点溶液中,c(Y-)+2c(OH-)=c(HY)+2c(H+)
C. HY中加NaOH溶液至pH=7 时,所得溶液中c(Y-)=c(Na+)=c(OH-)=c(H+)
D. 加入40 mL NaOH 溶液时,2c(Na+)=c(Y-)+c(HY)
【答案】B
【解析】根据图中信息可知,浓度均为0.1mol/L的两种酸HX、HY的pH分别为1和4,则HX为强酸,HY为弱酸。A.由于酸性HX![]() HY,当加入10mLNaOH溶液时,生成的NaX和NaY的物质的量相等,但Y-水解程度大,所以a点c(X-)>b点c(Y-),A错误;B.b点溶液中,NaY和HY的物质的量相等,根据电荷守恒可知:c(Na+)+c(H+)=c(Y-)+c(OH-),根据物料守恒可知:2c(Na+)=c(Y-)+c(HY),两等式合并消去c(Na+),可得c(Y-)+2c(OH-)=c(HY)+2c(H+),B正确;C. HY中加NaOH溶液至pH=7时,根据电荷守恒:c(Na+)+c(H+)=c(Y-)+c(OH-),可知c(Y-)=c(Na+),c(OH-)=c(H+),c(Na+)
HY,当加入10mLNaOH溶液时,生成的NaX和NaY的物质的量相等,但Y-水解程度大,所以a点c(X-)>b点c(Y-),A错误;B.b点溶液中,NaY和HY的物质的量相等,根据电荷守恒可知:c(Na+)+c(H+)=c(Y-)+c(OH-),根据物料守恒可知:2c(Na+)=c(Y-)+c(HY),两等式合并消去c(Na+),可得c(Y-)+2c(OH-)=c(HY)+2c(H+),B正确;C. HY中加NaOH溶液至pH=7时,根据电荷守恒:c(Na+)+c(H+)=c(Y-)+c(OH-),可知c(Y-)=c(Na+),c(OH-)=c(H+),c(Na+)![]() c(OH-),C错误;D. 加入40mLNaOH溶液时,溶液中NaY和NaOH的物质的量相等,根据物料守恒c(Na+)=2c(Y-)+2c(HY),D错误.答案选B.
c(OH-),C错误;D. 加入40mLNaOH溶液时,溶液中NaY和NaOH的物质的量相等,根据物料守恒c(Na+)=2c(Y-)+2c(HY),D错误.答案选B.


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】在一定温度下,向aL密闭容器中加入1molX气体和2molY气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是
2Z(g),此反应达到平衡的标志是![]()
A. 容器内压强不随时间变化
B. v正(X) =v逆(Z)
C. 容器内X、Y、Z的浓度之比为l:2:2
D. 单位时间内消耗0.1molX的同时生成0.2molZ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的 ( )
实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
V/mL | c/(molL﹣1) | V/mL | c/(molL﹣1) | V/mL | ||
A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,将纯Fe棒和石墨棒插入饱和食盐水中。下列说法正确的是

A. 如M接电源负极,N接电源正极,纯Fe棒不会被腐蚀,属于牺牲阳极的阴极保护法
B. 如M接电源正极,N接电源负极,将石墨棒换成Cu棒,电解质溶液换成CuSO4溶液,则可实现在纯Fe棒上镀铜
C. 如将M、N用导线直接相连,则纯Fe棒上产生气泡
D. 如将M、N用导线直接相连,一段时间后,向Fe电极区滴入2滴K3[Fe(CN)6]溶液,产生蓝色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】牡丹为中国的传统名花,有"花中之王"、"国色天香"之美誉。其花瓣细胞中,组成核酸的碱基、五碳糖、核苷酸的种类数分别是 ( )
A.5、2、8 B.4、2、2 C.5、2、2 D.4、4、8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组通过下列装置探究MnO2与FeCl3·6H2O能否反应产生Cl2。
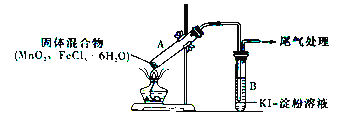
实验操作和现象如下表所示:
实验编号 | 操作 | 现象 |
实验1 | 按上图所示装置加热MnO2与FeCl3·6H2O混合物 | ①试管A中部分固体溶解,上方出现白雾 ②稍后,产生黄色气体,管壁附着黄色液滴 ③试管B中溶液变蓝 |
实验2 | 把试管A中的混合物换为FeCl3·6H2O,试管B中溶液换为KSCN溶液,加热 | 试管A中部分固体溶解,产生白雾和黄色气体;试管B中KSCN溶液变红 |
请回答下列问题:
(1)实验1和实验2 产生白雾的原因是_____________________________。
(2)实验2说明黄色气体中含有_____________(填化学式)。
(3)为进一步确认黄色气体中是否含有Cl2,该学习小组对实验1提出两种改进方案:
方案1:在试管A、B间增加盛有某种试剂的洗气瓶C,结果试管B 中溶液仍变为蓝色。
方案2:将试管B中KI-淀粉溶液替换为NaBr溶液,结果试管B 中溶液呈橙红色,且未检出Fe2+。则方案1中洗气瓶C 中盛放的试剂是_________;方案2 中检验Fe2+的试剂的名称是______,选择NaBr溶液后试管B中发生的主要反应的离子方程式为______________________________________。
(4)实验1充分加热后,若将试管A中产物分离得到Fe2O3 和MnCl2,则试管A 中产生Cl2 的化学方程式为__________________________________________。其尾气处理的方法是_______________________。
(5)该学习小组认为实验1中溶液变蓝,可能还有另外一种原因是__________________。请你设计实验方案验证此猜想_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【选修3——物质结构与性质】B、C、N、Si是几种常见的重要非金属元素,其形成的各种化合物在自然界中广泛存在。
(1)基态硅原子的电子排布式为________________________________。
B、C、N元素原子的第一电离能由大到小的顺序为______________________。
(2)BF3与一定量的水可形成如图所示晶体R。
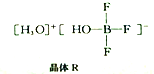
①晶体R中各种微粒间的作用力涉及___________(填字母代号)。
a.离子键 b.共价键 C.配位键 d.金属键 e.范德华力
②晶体R中阴离子的空间构型为___________________________。
(3)乙二胺(H2NCH2CH2NH3)与CuCl2溶液可形成配离子(结构如图所示),乙二胺分子中氮原子的杂化类型为_______。乙二胺和三甲胺[N(CH3)3]均属于胺,但乙二胺比三甲胺的佛点高得多,其原因是_______。
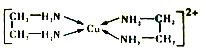
(4)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。它的晶体结构如图所示。六方相氮化硼是否含有π键?______(填“含”或“不含”),其质地软的原因是________________________________________,该物质能否导电?____________(填“能”或“不能”),其原因是______________________________。
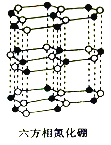
(5)SiC是原子晶体,其晶胞结构类似金刚石,假设正方体的边长为acm,估算SiC晶体的密度为______ g·cm-3(用含NA、a的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】普及化学知识有助于人们树立健康的观念.下列观念正确的是( )
A.天然物质都是绿色无毒的物质
B.只饮用纯净水有益人体健康
C.微量元素只能通过保健品摄入
D.植物油和动物脂肪要搭配食用
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJmol﹣1
②CH3OH(g)+ ![]() O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJmol﹣1
O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJmol﹣1
下列说法正确的是( )
A.CH3OH的燃烧热为192.9 kJmol﹣1
B.反应①中的能量变化如图所示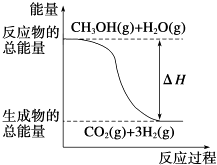
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应CH3OH(l)+ ![]() O2(g)═CO2(g)+2H2(g)的△H>﹣192.9 kJmol﹣1
O2(g)═CO2(g)+2H2(g)的△H>﹣192.9 kJmol﹣1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com