
反应mA(s)+nB(g)  pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是
pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是

①m+n>p
②x点表示的正反应速率大于逆反应速率
③n>p
④x点比y点时的反应速率慢
⑤若升高温度,该反应的平衡常数增大
A.①②⑤ B.只有②④ C.只有①③ D.只有①③⑤
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源:2017届山东省高三上第一次月考化学试卷(解析版) 题型:实验题
某化学兴趣小组在实脸室模拟侯德榜制碱法制备纯碱。主要步骤如下:
第一步:配制饱和NaCl溶液,倒入烧杯中加热;
第一步:控制温度在30-35 ℃。边搅拌边分批加入研细的NH4HCO3固体,加料完毕后,继续保温30分钟;
第三步:静置、过滤得NaHCO3晶体.用少量蒸馏水洗涤除去杂质,然后抽干;
第四步:将第二步所得固体转入蒸发皿中,灼烧2小时,制得纯碱固体,
已知:温度高于35℃时,NH4HCO3会分解。有关盐的溶解度(g/100g水)如下表:
盐 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | —— | —— | —— | —— |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.l | 12.7 | 14.5 | 16.4 | —— |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
回答下列问题:
(1)反应温度控制在30-35℃范围内,应采取的加热方法为 ,反应温度不能高于35℃的理由是 .
(2)第三步静置后析出NaHCO3晶体的原因是 ;用蒸馏水洗涤NaHCO3晶体的目的是除去杂质粒子 (用离子符号表示)。
(3)若向过滤所得母液中加入 (填写试剂名称),并作进一步处理,使NaCl溶液循环使用,同时可回收NH4Cl。
(4)纯碱产品不纯,含有NaHCO3、NaCl等杂质。测定纯碱中NaHCO3含量的方法是:准确称取纯碱样品Wg,放入锥形瓶中加蒸馏水溶解,加l-2滴酚酞指示剂,用物质的量浓度为cmol/L的盐酸滴定至溶液由红色到无色(指示CO32-+H+=HCO3-反应的终点), 所用盐酸体积为V1mL,再加1-2滴甲基橙指示剂,继续用盐酸滴定至溶液由黄变橙,所用盐酸总体积为V2mL。
① 实验室配制一定体积cmol/L盐酸需用的仪器除了容量瓶、烧杯、量筒外还需 ;在容量瓶的使用方法中,下列操作正确的是 (填写标号)
a.使用容量瓶前检验它是否漏水
b.容量瓶用蒸馏水洗净后,再用待配溶液润洗
c.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中.然后加蒸馏水定容
d.用容量瓶把溶液配制完成以后.直接贴上标签,放置备用
e.定容后盖好瓶塞,用食指顶住瓶塞,用另一只手指托住瓶底,把容量瓶倒转和摇动几次
② 写出纯碱样品中NaHCO3质量分数的计算式:NaHCO3 (%)= 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上第一次月考化学卷(解析版) 题型:实验题
(1)用量筒量取质量分数为98%,密度为1.84g/mL的浓硫酸_________mL.
(2)配制时,必须使用的仪器除烧杯、玻璃棒外,还缺少的仪器是_________、___________、_________。
(3)配制溶液过程中,操作不当会引起误差,分析下列操作对所配溶液浓度的影响。(用字母填空。A:偏高;B:偏低;C:无影响)
①量取浓硫酸时,仰视读数_________
②洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中__________
③没有洗涤稀释硫酸的烧杯和玻璃棒__________
④容量瓶不干燥___________
⑤定容时,仰视读数________
(4)从容量瓶中取该溶液40mL,与5mol/L的NaOH溶液_________mL恰好完全反应,反应后溶液中的c(Na+)=_________(忽略溶液混合过程中的体积变化).
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江佳木斯一中高一上第一次月考化学卷(解析版) 题型:选择题
下列分离或提纯物质的方法不正确的
A.用蒸馏法将海水淡化
B.用酒精萃取溴水中的溴
C.用升华法除去NaCl中含有的少量I2
D.用结晶法除去NaCl中混有的KNO3
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:填空题
肼(N2H6)又称联氨,是一种可燃性的液体,可用作火箭燃料。
(1)101kPa,32.0g N2H4在氧气中完全燃烧生成氮气,放出热量624kJ(25℃时),N2H4完全燃烧的热化学方程式是:
(2)肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20~30%的KOH溶液。肼—空气燃料电池放电时其负极的电极反应式是 。
(3)如右图是一个电化学过程示意图。

①铂片上发生的电极反应是 。
②假设使用肼—空气燃料电池作为本过程的电源,铜片质量变化128g,则肼—空气燃料电池理论上消耗标准状况下的空气 L(假设空气中氧气的体积含量为20%)。
(4)传统制备肼的方法是以NaClO氧化NH3制得肼的稀溶液,该反应的离子方程式是 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
在某恒温恒容的密闭容器内发生反应:2A(g)+B(g)  C(g);ΔH<0 。开始充入2 mol A和2 mol B,并达到平衡状态,下列说法正确的是
C(g);ΔH<0 。开始充入2 mol A和2 mol B,并达到平衡状态,下列说法正确的是
A.再充入2 mol A,平衡正移,A的转化率增大
B.如果升高温度,C的体积分数增大
C.如果增大压强,化学平衡一定向正方向移动,B的体积分数减小
D.再充入1 mol C,C的物质的量浓度将增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上10月检测化学卷(解析版) 题型:选择题
研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源。该电池以金属锂和钢板为电极材料,LiOH为电解质,使用时加入水即可放电。关于该电池的说法不正确的是
A.水既是氧化剂又是溶剂
B.放电时OH-向正极移动
C.放电时正极上有氢气生成
D.总反应为:2Li+2H2O=2LiOH+H2↑
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一上10月月考化学卷(解析版) 题型:选择题
在标准状况下,将A气体(不与水反应,摩尔质量是(Mg·mol-1)VL溶于0.5L水中,所得溶液的密度为ag·cm-3,则此溶液的物质的量浓度(mol·L-1)为
A.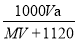 B.
B.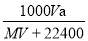 C.
C. D.
D.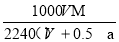
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省高二上10月月考化学卷(解析版) 题型:选择题
已知在1.01×105 Pa、298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是( )
A.2H2(g)+O2(g)=2H2O(l) ΔH=-484 kJ·mol-1
B.H2O(g)=H2(g)+ O2(g) ΔH=+242 kJ·mol-1
O2(g) ΔH=+242 kJ·mol-1
C.H2(g)+ O2(g)=H2O(g) ΔH=-484kJ·mol-1
O2(g)=H2O(g) ΔH=-484kJ·mol-1
D.2H2(g)+O2(g)=2H2O(g) ΔH=+484 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com