
 Cr2O72- (��ɫ)��H2O��
Cr2O72- (��ɫ)��H2O�� Cr3��(aq)��3OH��(aq)�������£�Cr(OH)3���ܶȻ�Ksp��10��32����c(Cr3��)����10��5 mol/L����Ϊc(Cr3��)�Ѿ���ȫ�������ֽ��ڢ۲���Һ��pH����4����ͨ������˵��Cr3���Ƿ������ȫ(��д���������)�� ��
Cr3��(aq)��3OH��(aq)�������£�Cr(OH)3���ܶȻ�Ksp��10��32����c(Cr3��)����10��5 mol/L����Ϊc(Cr3��)�Ѿ���ȫ�������ֽ��ڢ۲���Һ��pH����4����ͨ������˵��Cr3���Ƿ������ȫ(��д���������)�� ��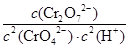


 ����ͬѧһ����ʦȫ�źþ�ϵ�д�
����ͬѧһ����ʦȫ�źþ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 B+C(g)-Q�ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ����
B+C(g)-Q�ﵽƽ�⡣��С������������´ﵽƽ��ʱ��C(g)��Ũ������С���ǰ��ƽ��Ũ����ȡ����·�����ȷ�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 I3-��aq����ijI2��KI�����Һ�У�I3-�����ʵ���Ũ��c��I3-�����¶�T�Ĺ�ϵ��ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������˵���в���ȷ����
I3-��aq����ijI2��KI�����Һ�У�I3-�����ʵ���Ũ��c��I3-�����¶�T�Ĺ�ϵ��ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������˵���в���ȷ���� 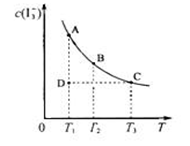
A����ӦI2��aq��+I-��aq�� I3-��aq���ġ�H��0 I3-��aq���ġ�H��0 |
| B�����¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1��K2 |
| C������Ӧ���е�״̬Dʱ��һ����v����v�� |
| D��״̬A��״̬B��ȣ�״̬B��c��I2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2SO3(g) ?H��?196kJ��moL?1�������ܱ��������м���岻�ܴ��������������ɻ���������ͼ��ʾͶ�ϣ�һ��ʱ��ﵽƽ��ʱ������˵����ȷ��
2SO3(g) ?H��?196kJ��moL?1�������ܱ��������м���岻�ܴ��������������ɻ���������ͼ��ʾͶ�ϣ�һ��ʱ��ﵽƽ��ʱ������˵����ȷ��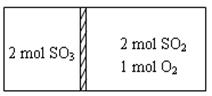
| A�����������£��ﵽƽ����������SO3�����������ͬ |
| B�����������£����������ߵ����ջ�ų���������ֵ֮��С��Ϊ196kJ |
| C��������Ϊ���ȣ��ﵽƽ��ʱ���ҷ�Ӧ���ʵ������ҷ�Ӧ���� |
| D��������Ϊ����������������SO2��ת����������SO3��ת����֮��С��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 cC(g)(��H<0)�ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯��������ͼ��ʾ��
cC(g)(��H<0)�ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯��������ͼ��ʾ��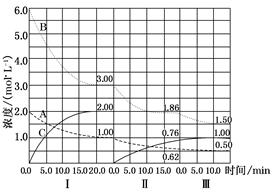
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 [Cu(NH3)3]CH3COO��CO(����ӦΪ���ȷ�Ӧ)
[Cu(NH3)3]CH3COO��CO(����ӦΪ���ȷ�Ӧ)�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ѧƽ�ⳣ���Ĵ�С���¶ȡ�Ũ�ȡ�ѹǿ�йأ�������� |
| B��Ka(HCN)<Ka(CH3COOH)˵����ͬ���ʵ���Ũ��ʱ������������Աȴ���ǿ |
| C�����Ȼ�����Һ�м���ͬŨ�ȵ�̼���ƺ���������Һ���Ȳ���BaSO4��������Ksp(BaSO4)>Ksp(BaCO3) |
| D�����¶�����ʱ�����ᡢ����ĵ��볣��(Ka��Kb)��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 xC(g)���ﵽƽ���C���������Ϊ��%����ά���������ݻ����¶Ȳ��䣬����ʼ���ʵ���A��0.6mol��B��0.3mol��C��1.4mol�����������ﵽƽ���C�����������Ϊ��%����xֵΪ
xC(g)���ﵽƽ���C���������Ϊ��%����ά���������ݻ����¶Ȳ��䣬����ʼ���ʵ���A��0.6mol��B��0.3mol��C��1.4mol�����������ﵽƽ���C�����������Ϊ��%����xֵΪ| A��ֻ��Ϊ2 | B��ֻ��Ϊ3 |
| C��������2��Ҳ������3 | D����ȷ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CH3OCH3(g)��H2O(g)����H����25 kJ/molij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���1 L���ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����£�
CH3OCH3(g)��H2O(g)����H����25 kJ/molij�¶��µ�ƽ�ⳣ��Ϊ400�����¶��£���1 L���ܱ������м���CH3OH����Ӧ��ijʱ�̲�ø���ֵ����ʵ���Ũ�����£�| ���� | CH3OH | CH3OCH3 | H2O |
| c/(mol��L��1) | 0.8 | 1.24 | 1.24 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com