
A、B、C、D代表4种元素,请完成下列问题
(1)A元素的基态原子的最外层有3个未成对电子,次外层有2个电子,A元素的名称是 ,该元素的原子核外共有 种不同运动状态的电子;该元素的第一电离能比后面一号元素大的原因是 。
(2)B为元素周期表中的29号元素,常与H2O、NH3等形成配合物。
B的无水硫酸盐晶体呈 色,向盛有B的硫酸盐 水溶液的试管里逐滴加入氨水,首先形成 ,继续添加氨水,沉淀溶解得到 ,写出后一步反应的离子方程式 。
(3)C元素的负一价离子的电子层结构与氩相同,C的最高价氧化物的水化物的化学式为 。
(4)A元素的最高价氧化物对应的水化物的稀溶液与29号元素的单质反应的离子方程式是____________________。
(5)D元素在元素周期表的各元素中,电负性仅小于氟,A的最低价氢化物与D的一种氢化物反应,生成的两种产物均不污染环境,其反应的化学方程式为___________________。
(1)氮;(1分)7;(1分)氮原子的最外层处于2s全充满,2p能级为半充满的 较稳定状态。(1分)
(2)白;(1分)蓝色沉淀;(1分)深蓝色溶液;(1分)
Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-(2分)(反应物中NH3写成NH3·H2O也可)
(3)HClO4(1分)
(4)3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O(2分)
(5)2NH3+3H2O2=N2+6H2O (2分)
【解析】
试题分析:(1)A元素的基态原子的最外层有3个未成对电子,次外层有2个电子,该元素电子排布只能为1s22s22p3,该元素为N元素。N元素核外共有7电子,故有7种不同运动状态的电子。该元素的第一电离能比后面一号元素大的原因是氮原子的最外层处于2s全充满,2p能级为半充满的 较稳定状态。
(2)29号元素为铜元素,无水硫酸盐晶体为无水硫酸铜,为白色。当想硫酸铜溶液中加入氨水,首先形成氢氧化铜蓝色絮状沉淀,继续加入氨水,沉淀溶解,形成配合物氢氧化二氨合铜,溶于水。离子方程式为Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-。
(3)C元素的负一价离子的电子层结构与氩相同,即该元素为17号元素,氯元素。则其最高价氧化物的水化物为HClO4
(4)A元素为氮元素,最高价氧化物对应的水化物的稀溶液为稀硝酸,29号元素为铜元素,故,其离子反应方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
(5)D元素在元素周期表的各元素中,电负性仅小于氟,则D为氧元素。A为氮元素,其最低价氢化物为NH3,D的氢化物有H2O、H2O2两种,能有氨气发生反应的只有H2O2。故,其反应方程式为2NH3+3H2O2=N2+6H2O 。
考点:元素周期律、电负性、离子反应方程式、原子核外电子排布。


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
 (2009?辽宁)下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略.)
(2009?辽宁)下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物.(反应条件图中已省略.)查看答案和解析>>
科目:高中化学 来源: 题型:




| 元素编号 元素性质 |
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| 最低负化合价 | -2 | -3 | -1 | -3 |
| ||
| ||


查看答案和解析>>
科目:高中化学 来源: 题型:
下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色的固体化合物。(反应条件图中已省略)
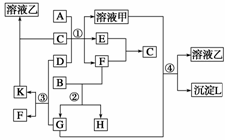
(1)A、B、C、D代表的物质分别为
___________________、 、 、 (填化学式);
(2)反应①中的C、D均过量,该反应的化学方程式是
________________________________________________________________________;
(3)反应②中,若B与F的物质的量之比为4∶3,G、H分别是 、 (填 化学式);
(4)反应③中产物K的化学式为 ;
(5)反应④的离子方程式为
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图表示有关物质(均由短周期元素形成)之间的转化关系,其中A为常见的金属单质,B为非金属单质(一般是黑色粉末),C是常见的无色无味液体,D是淡黄色
的固体化合物。(反应条件图中已省略。)
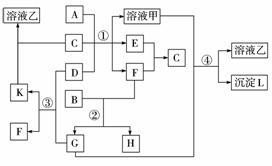
(1)A、B、C、D代表的物质分别为____________、____________、__________、____________(填化学式);
(2)反应①中的C、D均过量,该反应的化学方程式是____________ ____________ ;
(3)反应②中,若B与F物质的量之比为4∶3,G、H分别是____________、____________(填化学式);
(4)反应③产物中K的化学式为____________;
(5)反应④的离子方程式为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com