
设C+CO2 2CO(正反应吸热),反应速率为v1;N2+3H2
2CO(正反应吸热),反应速率为v1;N2+3H2 2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为( )
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为( )
A.同时增大 B.同时减小 C.v1增大,v2减小 D.v1减小,v2增大
科目:高中化学 来源:2015-2016学年黑龙江大庆一中高二下第二次段考化学试卷(解析版) 题型:选择题
只用一种试剂,区别二甲苯、四氯化碳、庚烯、乙醇、碘化钠溶液、亚硫酸六种无色液体,应选用( )
A.双氧水 B.溴水 C.氢氧化钠溶液 D.硝酸银溶液
查看答案和解析>>
科目:高中化学 来源:2015-2016学年宁夏中卫一中高一下第三次月考化学试卷(解析版) 题型:选择题
制取氯乙烷(CH3—CH2Cl)的最好方法是
A.乙烷与氯气发生取代反应 B.乙烯与氯气发生加成反应
C.乙烯与氯化氢发生加成反应 D.甲烷与氯气发生取代反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古平煤高中高一实验班下期中化学卷(解析版) 题型:选择题
碱性电池具有容量大,放电电流大的特点,因而得到广泛应用。锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s),下列说法错误的是( )
A.电池工作时,锌失去电子
B.电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e-═Mn2O3(s)+2OH-(aq)
C.电池工作时,电子由正极通过外电路流向负极
D.外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古平煤高中高一实验班下期中化学卷(解析版) 题型:选择题
已知短周期元素的离子aA2+、bB+、cC2-、dD-都具有相同的电子层结构,则下列叙述正确的是( )
A.原子半径:A>B>D>C
B.原子序数:d>c>b>a
C.离子半径:C2->D->B+>A2+
D.单质的还原性:A>B>D>C
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁庄河高中高一下期中化学试卷(解析版) 题型:实验题
以下是有关SO2、Cl2的性质实验。
(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质。
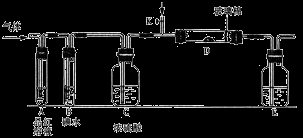
①若从左端分别通入SO2和Cl2,装置A中观察到的现象 (填“相同”或“不相同”);若装置D中装的是V2O5(催化剂)。通入SO2时,打开K通入适量O2的化学反应方程式为 。
②SO2通入B中,溶液颜色褪去,则该反应的离子方程式为 。
(2)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入加量(填字母) ,能产生白色沉淀。
A.氨水 B.稀盐酸 C.硝酸钾溶液 D.氯化钠溶液
(3)若由元素S和O组成-2价酸根离子X,X中S和O的质量比为2∶3;当Cl2的与含X的溶液完全反应后,得澄清溶液,取少量该溶液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。写出Cl2与含X的溶液反应的离子方程式 。
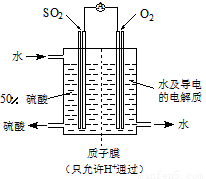
(4)某科研单位利用电化学原理用SO2来制备硫酸,装置如图,含有某种催化剂,电极为多孔的材料,能吸附气体,同时也能使气体与电解质溶液充分接触。通入SO2的电极为 极,其电极反应式为 ;电池的总反应式 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁庄河高中高一下期中化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为16。Y的原子半径比X的大,X 与W 同主族,Z 是地壳中含量最高的金属元素。下列说法正确的是( )
A.原子半径的大小顺序:r(W)>r(Z)>r(Y)
B.Y、W最高价氧化物对应水化物均能溶解Z的氢氧化物
C.元素W的简单气态氢化物的热稳定性比X的强
D.元素X、Y只能形成一种化合物
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽六安一中高一下周末作业四化学试卷(解析版) 题型:填空题
化学与人类生产和生活中密切相关,掌握有关的化学基础知识可以改善我们的生活。
【I】日常生活中使用的各种电池就是利用化学反应将化学能转化为电能,各种各样的电池的发展是化学对人类的一项重大贡献。请回答下列有关化学电源的问题:
(1)下列有关电池的叙述中正确的是___________。
A.锌锰干电池工作一段时间后碳棒变细 B.氢氧燃料电池可将热能直接转变为电能
C.甲烷燃料电池工作时甲烷在负极被氧化 D.太阳能电池的主要材料是高纯度的二氧化硅
(2)锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过。下列有关叙述正确的是( )
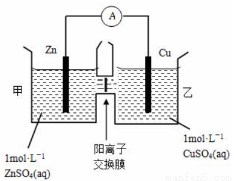
A.铜电极上发生氧化反应
B.电池工作一段时间后,甲池的c(SO42-)减小
C.电池工作一段时间后,乙池溶液的总质量增加
D.甲池中的阳离子向乙池移动,保持溶液中电荷平衡
【II】自来水厂生产自来水时,需要用到净水剂,对水进行消毒杀菌处理。
(3)高铁酸钾(K2FeO4)是一种新型多功能水处理剂。工业上有多种方法制备高铁酸钾,其中一种方法是在氢氧化钾溶液中用次氯酸钠氧化氢氧化铁。该反应的可用离子方程式表示为___________。
(4)用高铁酸钾和锌制成的高铁碱性电池,能储存比普通碱性电池多50%的电能,己知该电池的总反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,则负极的电极反应是______________。
查看答案和解析>>
科目:高中化学 来源:2016年全国普通高等学校招生统一考试化学(江苏卷参考版) 题型:选择题
化合物X是一种医药中间体,其结构简式如图所示。下列有关化合物X的说法正确的是
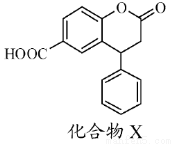
A.分子中两个苯环一定处于同一平面
B.不能与饱和Na2CO3溶液反应
C.在酸性条件下水解,水解产物只有一种
D.1 mol化合物X最多能与2 molNaOH反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com