
 种:Na+、NH4+、Fe3+、Cu2+、Mg2+、Cl-、SO42-。现做以下实验:
种:Na+、NH4+、Fe3+、Cu2+、Mg2+、Cl-、SO42-。现做以下实验: 子方程式是:
子方程式是: 科目:高中化学 来源:不详 题型:单选题
| A.该溶液中一定不含钾元素 | B.该溶液中不可能含钠的化合物 |
| C.该溶液中不可能含钠单质 | D.该溶液中可能含钠的化合物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使紫色石蕊试液变红的溶液中:Fe2+、Cu2+、Cl-、NO3-能够大量共存 |
| B.加入铝粉放出H2的溶液中:Na+、Mg2+、HCO3-、SO42-不能大量共存 |
| C.常温下,醋酸钠与醋酸的混合液PH=7:则c(Na+)= c(CH3COO-) |
| D.0.1mol/L NaHCO3溶液中:c(Na+)= c(HCO3-)+ c(CO32-)+ c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1mol/L醋酸溶液中:c(H+) = c(CH3COO- ) +c(OH- ) |
| B.中和pH与体积都相同的硫酸和醋酸,消耗NaOH的量后者大于前者 |
| C.由水电离的H+浓度为1.0×10-4mol/L的溶液,pH一定等于4 |
| D.NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3) >c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、K+、Cl-、CO32- | B.Cu2+、Na+、SO42-、NO3- |
| C.Ba2+、K+、Cl-、SO42- | D.K+、Na+、HCO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 .24升(标准状态)氨气通入250mL浓度为0.1mol·L-1的硫酸溶液中,充分反应后溶液中各离子浓度由大到小的顺序为 。
.24升(标准状态)氨气通入250mL浓度为0.1mol·L-1的硫酸溶液中,充分反应后溶液中各离子浓度由大到小的顺序为 。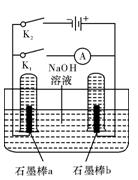
 路中有电流通过。写出a极的电极反应式 。
路中有电流通过。写出a极的电极反应式 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
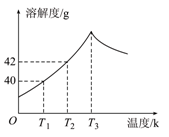
| A.小于40g | B.等于40g | C.等于42g | D.大于42g |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Cu2+、NO3-、CO32- | B.Al 3+、K+、Cl-、HCO3- |
| C.Fe2+、 Na+、SO42-、NO3- | D.Mg2+、NH4+、SO42-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com