
实验室可用NaBr、浓H2SO4和乙醇为原料制备溴乙烷,已知反应物的用量:0.3mol NaBr(s);0.25mol乙醇;36mL浓硫酸(溶质分数为98%,密度1.84g×mL-1);25mL水,其中乙醇的密度为0.80g×cm-3,回答下列问题。
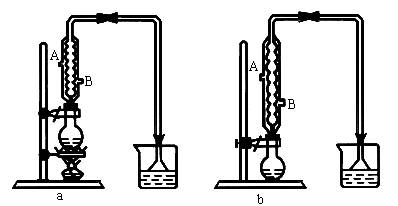
(1)该实验应选择图中的a还是b装置?
___________________________________________________
(2)反应装置中的烧瓶应选择下列哪种规格最合适?
__________________________
A.50 mL B.100mL C.150mL D.250mL
(3)冷凝管中的冷凝水的流向应是_____________。
A.A进B出 B.B进A出 C.从A进或B进均可
(4)由NaBr浓H2SO4和乙醇共热制备C2H5Br反应的化学方程式为_________________
________________。可能发生的副反应为:_____________________________________。
(5)上述实验完成后,需要将烧瓶中的有机物蒸馏出来,所得馏出液中含有_____________________________________________________________。
(6)从棕黄色的粗溴乙烷制取无色的溴乙烷应加入的试剂是__________________,必须使用的仪器是_______________________________。
(7)本实验的产率为60%,则可制取溴乙烷______________g。
(8)为除去溴乙烷中残留的少量水,可选用无水CaCl2作干燥剂,并蒸馏。为证明最终得到的产品一溴乙烷中含有溴元素,可采取的实验方法是_____________________________
__________________________________________________。
(1)a装置 (2)C (3)B (4)NaBr+H2SO4+C2H5OH (2)选择反应器烧瓶规格的原则是:反应物体积应介于烧瓶容积的 (7)问中要考虑反应物过量的问题: nH2SO4= 由NaBr+H2SO4+C2H5OH→NaHSO4+C2H5Br+H2O 0.30(过量) 0.25mol 则理论上可生成0.25molC2H5Br,又考虑本实验产率为60%,故可生成C2H5Br:0.25mol´109g×mol-1´60%=16.35g。
|


科目:高中化学 来源: 题型:
 实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:| 浓H2SO4 |
| △ |
| 浓硫酸 |
| 140℃ |
| 浓硫酸 |
| 140℃ |
| ||
| ||
| △ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
![]()
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为
(1)该实验应选择图中的a装置还是b装置?____________________________________。

(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50 Ml B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是( )
A.A进B出 B.B进A出 C.从A进或B进均可
(4)可能发生的副反应为:________________、________________、________________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
![]()
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试完成下列问题。
(1)该实验应选择图中的a装置还是b装置?____________________________________。

(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50 Ml B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是( )
A.A进B出 B.B进A出 C.从A进或B进均可
(4)可能发生的副反应为:________________、________________、________________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBrC2H5Br+H2O
已知反应物的用量为:0.30mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。
(1)该实验应选择图中的a装置还是b装置?_____________。
(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50mL B.100mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是 ( )
A. A进B出 B. B进A出 C. 从A进或B进均可
(4)可能发生的副反应为:_____________、__________、______________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是_______ _________。A、浓NaOH溶液 B、Na2SO3溶液 C、CCl4 D、水
查看答案和解析>>
科目:高中化学 来源:2013届山西省高二3月月考化学试卷(解析版) 题型:实验题
实验室可用NaBr、浓H2SO4、乙醇为原料制备少量溴乙烷:
C2H5—OH+HBr C2H5Br+H2O
C2H5Br+H2O
已知反应物的用量为:0.30 mol NaBr(s);0.25 mol C2H5OH(密度为0.80 g·cm-3);36 mL浓H2SO4(质量分数为98%,密度为1.84 g·mL-1);25 mL水。试回答下列问题。

(1)该实验应选择图中的a装置还是b装置?_____________。
(2)反应装置中的烧瓶应选择下列哪种规格最合适( )
A.50 mL B.100 mL C.150 mL D.250 mL
(3)冷凝管中的冷凝水的流向应是 ( )
A. A进B出 B. B进A出 C. 从A进或B进均可
(4)可能发生的副反应为:_____________、__________、______________(至少写出3个方程式)。
(5)实验完成后,须将烧瓶内的有机物蒸出,结果得到棕黄色的粗溴乙烷,欲得纯净溴乙烷,应采用的措施是_______ _________。A、浓NaOH溶液 B、Na2SO3溶液 C、CCl4 D、水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com