
| A. | 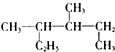 的系统命名是3,4-二甲基己烷 的系统命名是3,4-二甲基己烷 | |
| B. | 樱桃中含有一种羟基酸(如图所示)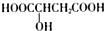 ,该羟基酸可以发生取代、氧化和缩聚等反应 ,该羟基酸可以发生取代、氧化和缩聚等反应 | |
| C. | 所有的糖、油脂、蛋白质都能水解,但水解产物不同 | |
| D. | 等质量的甲醛和乙酸充分燃烧耗氧量相同 |
分析 A.最长碳链含6个C,3、4号C上有甲基;
B.含-OH、-COOH;
C.单糖不能水解,且油脂水解生成高级脂肪酸(或盐)、甘油,蛋白质水解生成氨基酸;
D.甲醛和乙酸的最简式均为CH2O.
解答 解:A.最长碳链含6个C,3、4号C上有甲基,则名称为3,4-二甲基己烷,故A正确;
B.含-OH、-COOH,可发生取代、缩聚反应,且含-OH可发生氧化反应,故B正确;
C.单糖不能水解,且油脂水解生成高级脂肪酸(或盐)、甘油,蛋白质水解生成氨基酸,糖类水解可生成单糖,故C错误;
D.甲醛和乙酸的最简式均为CH2O,含C、H、O量相同,则等质量的甲醛和乙酸充分燃烧耗氧量相同,故D正确;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质、有机物的组成、有机反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源: 题型:选择题
| A. | 18g冰晶体中含有氢键的数目为2NA | |
| B. | 1molH2O2中含有非极性键的数目为NA | |
| C. | 1molSiO2晶体中含有Si-O键的数目为4NA | |
| D. | 22.4LHF(标准状况)中含有氟原子的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该电池的负极锌发生还原反应 | |
| B. | 该电池反应中二氧化锰起催化剂作用 | |
| C. | 当0.lmol Zn完全溶解时,流经电解液的电子个数约为1.204×1023 | |
| D. | 电池正极反应式为 MnO2+e-+H20═MnO(OH)+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
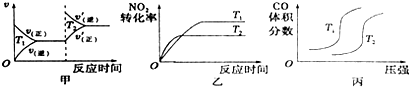
| 浓度/mol.L-1/时间/min | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
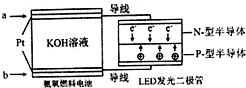
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl•在反应中是催化剂 | |
| B. | Cl•比Cl2更活泼 | |
| C. | ②也可能是Cl•(g)+CH4(g)→CH3Cl(g)+H•(g) | |
| D. | 由③可知C-Cl的键能比Cl-Cl的键能小 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

难溶物 | NiS | ZnS | CuS | CaF2 | MgF2 |
| 溶度积常数 | 1.07×10-21 | 2.93×10-25 | 1.27×10-36 | 1.46×10-10 | 7.42×10-11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 古诗或谚语 | 含有的化学反应类型 |
| A | 爆竹声中除旧岁,春风送暖入屠苏 | 复分解反应 |
| B | 千锤万凿出深山,烈火焚烧若等闲 | 分解反应 |
| C | 春蚕到死丝方尽,蜡炬成灰泪始干 | 化合反应 |
| D | 真金不怕火,怕火便是铜 | 置换分解反应 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H10含苯环的烃同分异构体有3种 | |
| B. | 结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物,其单体是乙烯 | |
| C. | 苯中含有杂质苯酚,可用浓溴水来除杂 | |
| D. | 丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,它们与氢气充分反应后的产物是同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2比O2的化学性质稳定 | B. | F2、Cl2、Br2、I2的沸点逐渐升高 | ||
| C. | 金刚石的熔点比晶体硅高 | D. | HF、HCl、HBr、HI的热稳定性依减弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com