分析:首先判断单质或化合物的类型,离子化合物阴离子带电荷且用“[]”,共价化合物不带电荷,注意各原子或离子满足稳定结构,分析所给微粒类型,根据化学键类型及原子间形成共用电子对数目,根据电子式书写的规则作答.
解答:解:A、氢气中两个H原子以共价键结合在一起,其电子式为H:H,故A正确;
B、N
2为非金属单质,N原子之间有3各共用电子对,电子式为

,故B错误;
C、氯化钠为离子化合物,氯离子带电荷并需用方括号括起来,钠离子用离子符号表示,氯化钠的电子式为
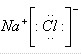
,故C正确;
D、H
2O为共价化合物,H与O以共价键相结合,电子式为

,故D正确;
故选:B.
点评:本题考查常用化学用语的书写,难度较小,注意:①阴离子的电子式要用[]括起来并在右上角标明电荷,阳离子的电子式除铵离子外,一般与阳离子符号相同;②注意4类电子式:阳离子的电子式、阴离子的电子式、原子的电子式、分子的电子式.

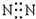
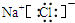

 ,故B错误;
,故B错误;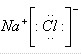 ,故C正确;
,故C正确; ,故D正确;
,故D正确;

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案