
用硫酸酸化的三氧化铬(CrO3)遇酒精后,其颜色由红色变为蓝绿色(反应如下),用此反应可测得司机是否是酒后驾车。此反应的氧化剂是( )
2CrO3+3C2H5OH+3H2SO4=Cr2(SO4)3+3CH3CHO+6H2O
A.H2SO4 B.CrO3 C.Cr2(SO4)3 D.C2H5OH
科目:高中化学 来源:2014年高考化学苏教版总复习 11-1 认识有机化合物练习卷(解析版) 题型:选择题
某化合物的结构(键线式)及球棍模型如下:
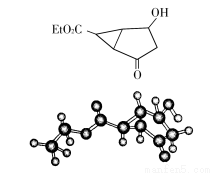
该有机分子的核磁共振波谱图如下(单位是ppm)。

下列关于该有机物的叙述不正确的是( )
A.该有机物不同化学环境的氢原子有8种
B.该有机物属于芳香族化合物
C.键线式中的Et代表的基团为—CH2CH3
D.1 mol该有机物完全燃烧可以产生6 mol水
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 10-2 物质的检验、分离和提纯练习卷(解析版) 题型:填空题
有一瓶澄清的溶液,其中可能有NH4+、K+、Na+、Mg2+、Ba2+、Al3+、Cl-、I-、NO3-、CO32-、S2-、SO42-、AlO2-、MnO4-,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈强酸性,可以排除________离子的存在;
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4层呈紫色,可以排除________离子的存在;
(3)另取出部分溶液逐滴加入NaOH溶液,使溶液从酸性逐渐变为碱性,在滴加过程中和滴加完毕后,溶液均无沉淀产生,则又可以排除________离子的存在;
(4)取出部分上述碱性溶液滴加Na2CO3溶液后,有白色沉淀生成,证明________离子存在,又可排除________离子的存在;
(5)将(3)得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。根据上述实验事实确定:该溶液中肯定存在的离子是________,还不能确定是否存在的离子是________。
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-4 氧化还原反应练习卷(解析版) 题型:填空题
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。
(1)已知KBrO3在反应中得到电子,则该反应的还原剂是 。
(2)已知0.2 mol KBrO3在反应中得到1 mol电子生成X,则X的化学式为 。
(3)根据上述反应可推知
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的计量数填入下列方框中,并标出电子转移的方向和数目。
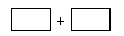
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-4 氧化还原反应练习卷(解析版) 题型:选择题
下列氧化还原反应中,实际参加反应的氧化剂与还原剂的物质的量之比正确的是( )
①KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O;1:6
②Fe2O3+2Al Al2O3+2Fe;1:2
Al2O3+2Fe;1:2
③SiO2+3C=SiC+2CO↑;1:2
④3NO2+H2O=2HNO3+NO;2:1
A.①③ B.②③ C.②④ D.①④
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-3 溶液的配制及分析练习卷(解析版) 题型:选择题
已知NH3和HCl都是能用来做喷泉实验的气体。若在同温同压下用等体积的一个烧瓶收集满NH3,另一个收集HCl气体未满,喷泉实验停止后,两个烧瓶内溶液的关系是(不考虑溶质的扩散及静止时液面高度的影响)( )
A.溶质的物质的量浓度相同、溶质的质量分数不同
B.溶质的质量分数相同、溶质的物质的量浓度不同
C.溶质的物质的量浓度和溶质的质量分数都不同
D.溶质的物质的量浓度和溶质的质量分数都相同
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-3 溶液的配制及分析练习卷(解析版) 题型:选择题
用98%的浓硫酸(密度为1.84 g·cm-3)配制1 mol·L-1的稀硫酸100 mL,配制溶液时可能用到的仪器有①玻璃棒;②胶头滴管;③100 mL容量瓶;④托盘天平;⑤50 mL烧杯;⑥10 mL量筒。则正确的选用顺序是( )
A.⑥③⑤①② B.⑥⑤③①②
C.④⑤③②① D.⑥⑤①③②
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版总复习 1-2 物质的量、物质的聚集状态练习卷(解析版) 题型:选择题
标准状况下,a L气体X2和b L气体Y2恰好完全反应生成c L气体Z,若2a=6b=3c,则Z的化学式为( )
A.XY2 B.X2Y C.X3Y D.XY3
查看答案和解析>>
科目:高中化学 来源:2014年高考化学苏教版一轮复习3-1钠、镁及其化合物练习卷(解析版) 题型:填空题
纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图。
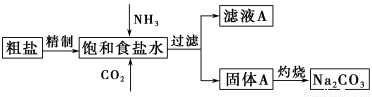
已知:向饱和食盐水中通入NH3、CO2后发生的反应为NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+、Mg2+、SO42-等。
精制除杂的步骤顺序是a→ → → →b(填字母编号)。
a.粗盐溶解,滤去沉渣
b.加入盐酸调pH
c.加入Ba(OH)2溶液
d.加入Na2CO3溶液
e.过滤
向饱和食盐水中先通入NH3,后通入CO2,理由是 。
(2)灼烧固体A制Na2CO3在 (填字母序号)中进行。
a.坩埚 b.蒸发皿 c.烧杯 d.锥形瓶
证明滤液A中含有NH4+的方法是 。
对滤液A进行重结晶能够获得NH4HCO3,向pH=13含Na+、K+的溶液中加入少量NH4HCO3使pH降低,反应的离子方程式为 。
(3)下图装置中常用于实验室制备CO2的是 (填字母编号);用b装置制备NH3,分液漏斗中盛放的试剂是 (填试剂名称),烧瓶内可加入的固体试剂是 (填试剂名称)。
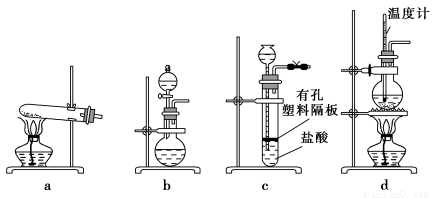
(4)一种天然碱晶体成分是aNa2CO3·bNa2SO4·cH2O,某同学利用下列提供的试剂,设计了如下简单合理测定Na2CO3的质量分数的实验方案。(仪器自选)请把实验方案填全:
供选择的试剂:1.0 mol·L-1 H2SO4溶液、1.0 mol·L-1 BaCl2溶液、稀氨水、碱石灰、Ca(OH)2溶液、蒸馏水
①称取m1g天然碱晶体样品,溶于适量蒸馏水中。
② 。
③ 。
④计算天然碱晶体中含Na2CO3的质量分数。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com