
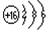 ;A为Na,离子的结构示意图为
;A为Na,离子的结构示意图为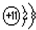 ,Na与S形成化合物的化学式是Na2S,它的电子式是
,Na与S形成化合物的化学式是Na2S,它的电子式是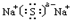 ,它属于离子化合物,锂与氧气反应生成氧化锂,化学反应方程式为:4Li+O2
,它属于离子化合物,锂与氧气反应生成氧化锂,化学反应方程式为:4Li+O2
| ||
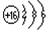 ;
;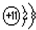 ; Na2S,
; Na2S,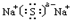 ,离子;4Li+O2
,离子;4Li+O2
| ||


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 用途 | 解释 | |
| A | SO2可用于漂白纸浆 | SO2具有氧化性 |
| B | 明矾可用于净水 | 明矾在水中生成的氢氧化铝胶体有吸附性 |
| C | 纯碱可去油污 | 纯碱水解呈碱性 |
| D | “84”消毒液可用于漂白 | 置于空气中生成的次氯酸有氧化性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、25℃时,0.1 mol/L HF溶液pH=1 |
| B、Ksp(CaF2)随温度和浓度的变化而变化 |
| C、向反应后的溶液中继续加入100m L 0.1 mol/L Na2CO3有CaCO3沉淀产生 |
| D、该体系中有CaF2沉淀产生,且反应后溶液中的F-浓度为1×10-4.5mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
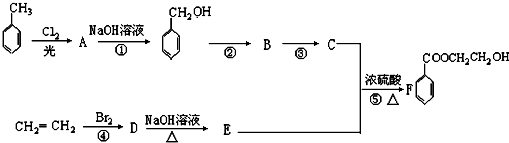
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(A)=0.01 mol/(L?s) |
| B、v(B)=0.04 mol/(L?s) |
| C、v(B)=0.60mol/(L?min) |
| D、v(C)=1.0mol/(L?min) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com