
一定温度下,在溶剂为1L的密闭容器内放入2mol 和8mol
和8mol ,发生如下反应
,发生如下反应
 ,反应中
,反应中 的物质的量随反应时间变化的曲线如下图,按下列要求作答:
的物质的量随反应时间变化的曲线如下图,按下列要求作答:
(1)在该温度下,反应的化学平衡常数表达式为:
(2)若 ,计算从
,计算从 至
至 时以
时以 表示的反应速率:
表示的反应速率:
mol·L-1·s-1
(3)图中 哪一个时刻表示反应已经达到平衡?答:
哪一个时刻表示反应已经达到平衡?答:
(4) 时,正反应速率 (填“>”、“<”或“=”)逆反应速率
时,正反应速率 (填“>”、“<”或“=”)逆反应速率
(5)维持容器的温度不变,若缩小容器的体积,则平衡向 移动(填“正反应方向”、“逆反应方向”或“不变”)
(6)维持容器的体积不变,升高温度,达到新平衡时体系的颜色 (填“变深”、“变浅”或“不变”)
科目:高中化学 来源: 题型:
草酸是二元弱酸,草酸氢钾溶液呈酸性。在0.1mol·L-1 KHC2O4溶液中,下列关系正确的是
A.c(K+)+c(H+)=c(HC2O4-)+c(OH-)+c(C2O42-)
B.c(HC2O4-)+c(C2O42-)=0.1mol·L-1
C.c(C2O42-)>c(H2C2O4)
D.c(K+)=c(H2C2O4)+c(HC2O4-)+c(C2O42-)
查看答案和解析>>
科目:高中化学 来源: 题型:
2013年1月27日百度新闻资讯中报道,活性氧化锌是一种多功能性的新型无机材料,其颗粒大小约在1~100纳米。云南化工冶金研究所采用湿化学法(NPP-法)制备纳米级活性氧化锌,可用各种含锌物料为原料,采用酸浸出锌,经过多次净化除去原料中的杂质,然后沉淀获得碱式碳酸锌,最后焙解获得活性氧化锌,化学工艺流程如下:

通过________可以检验流程中滤液2中含有Na+,该实验的具体操作是
。
(2)上述流程图中pH=12的Na2CO3溶液中c(CO )=0.50 mol/L,c(HCO
)=0.50 mol/L,c(HCO )=1×10-2 mol/L,则c(Na+)∶c(OH-)=______________________。
)=1×10-2 mol/L,则c(Na+)∶c(OH-)=______________________。
(3)“溶解”后得到的酸性溶液中含有Zn2+、SO ,另含有Fe2+、Cu2+等杂质。先加入_______(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2。经检测溶液中Fe2+的浓度为0.009 mol·L-1,则每升溶液中至少应加入________mol KMnO4。
,另含有Fe2+、Cu2+等杂质。先加入_______(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2。经检测溶液中Fe2+的浓度为0.009 mol·L-1,则每升溶液中至少应加入________mol KMnO4。
(4)已知常温下,Cu(OH)2的溶度积常数Ksp=2×10-20。溶液中杂质Cu2+浓度为0.002 mol·L-1,若要生成沉淀,则应调节溶液的pH大于________。
(5)“沉淀”得到ZnCO3·2Zn(OH)2·H2O,“煅烧”在450~500 ℃下进行,“煅烧”反应的化学方程式为: ___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中发生如下反应:mA(g)+nB(g)  pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是 ( )
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是 ( )
A. 平衡向逆反应方向移动 B. A的转化率降低 C. m+n>p D.C的体积分数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右下图。下列有关该氢氧燃料电池的说法错误的是
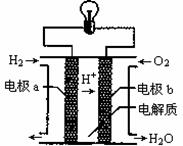 A.该电池工作时将化学能转化为电能
A.该电池工作时将化学能转化为电能
B.电流从电极b经外电路流向电极a
C.该电池中的电极b是正极
D.在电极a上发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
对金属制品进行抗腐蚀处理,可延长其使用寿命。
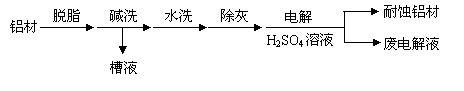 (1)以下为铝材表面处理的一种方法:
(1)以下为铝材表面处理的一种方法:
① 碱洗的目的是除去铝材表面的自然氧化膜,为将碱洗槽液中铝以沉淀形式回收,最好向槽液中加入下列试剂中的 。
a.NH3 b.CO2 c.NaOH d.HNO3
②以铝材为阳极,在H2SO4 溶液中电解,铝材表面形成氧化膜,阳极电极反应为
。取少量废电解液,加入NaHCO3,溶液后产生气泡和白色沉淀,产生沉淀的原因是 。
(2)镀铜可防止铁制品腐蚀,电镀时用铜而不用石墨作阳极的原因是 。
(3)利用下图装置,可以模拟铁的电化学防护。
若X为碳棒,为减缓铁的腐蚀,开关K应置于 处。若X为锌,开关K置于 处。

查看答案和解析>>
科目:高中化学 来源: 题型:
储氢合金表面镀铜过程发生反应Cu2++2HCHO+4OH-=Cu +H2
+H2 +2H2O+2HCOO-,下列说法错误的是
+2H2O+2HCOO-,下列说法错误的是
A.电镀过程中氢气在镀件表面析出
B.电镀时溶液中Cu2+移向阴极,并在阴极上发生还原反应
C.阳极反应式为HCHO+3OH--2e-=2H2O+HCOO-
D.电镀时每生成6.4g铜镀层放出2.24L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
常温条件下,下列各组离子在指定溶液中能大量共存的是
A.使石蕊试液变红的溶液中:Fe2+、NO 、SO42—、Na+
、SO42—、Na+
B.由水电离出的c(H+)=1×10-14mol/L的溶液中:Ca2+、Cl-、HCO 、K+
、K+
C.c(H+)/c(OH-)=1×1012的溶液中:NH 、Cl-、SO42—、Al3+
、Cl-、SO42—、Al3+
D.c(Al3+)=0.1 mol/L的溶液中:K+、Cl-、SO42—、CO32-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com