
【题目】在一定条件下Na2CO3溶液存在水解平衡:CO32-+H2O![]() HCO3-+OH-。下列说法正确的是
HCO3-+OH-。下列说法正确的是
A. Na2CO3溶液中:2c(Na+)= c(CO32-)+ c(HCO3-)+ c(H2CO3)
B. 加入NaOH固体,溶液中c(Na +)和c(CO32-)都增大
C. 稀释Na2CO3溶液,溶液中的离子浓度都减少
D. 升高温度,Na2CO3溶液pH减小
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于苯的叙述正确的是( )

A. 反应①为取代反应,有机产物的密度比水小
B. 反应②为氧化反应,反应现象是火焰明亮并带有较多的黑烟
C. 反应③为取代反应,有机产物是一种烃
D. 反应④1mol苯最多与3molH2发生加成反应,是因为苯分子含有三个碳碳双键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验测得某碳氢化合物A中含碳80%,含氢20%,该化合物的实验式是__________,又测得该化合物的相对分子质量是30,该化合物的分子式______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物F是治疗感冒药的主要成分之一,其合成路线如下:

已知:
① (R、R'、R"均代表烃基;X代表卤素原子);
(R、R'、R"均代表烃基;X代表卤素原子);
②A蒸气的密度是相同条件下氢气密度的53倍。
请回答下列问题:
(1)D中官能团的名称为______。
(2)E的结构简式为____________。
(3)写出反应②的化学方程式:___________________。
(4)B的消去反应产物可以用于合成高分子化合物G,G的结构简式是________;若G的平均相对分子质量为9000,则其平均聚合度约为___________(保留整数)。
(5)符合下列条件的C的同分异构体有________种(考虑顺反异构)
①能与氢氧化钠溶液反应 ②分子中含有两种官能团。
任写一种存在顺反异构的同分异构体的结构简式__________(写反式结构);
(6)C的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同_____(填字母序号)。
A.核磁共振仪 B.元素分析仪 C.质谱仪 D.红外光谱仪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属钠的叙述正确的是( )
A. 金属钠可以保存在煤油中
B. 金属钠着火时,可用水来灭火
C. 钠与硫酸铜溶液反应可置换出铜
D. 实验时用剩的钠块不能放回原试剂瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中完全正确的一组是( )
①常温常压下,1 mol甲基(—CH3)所含的电子数为10NA
②由Cu、Zn和稀硫酸组成的原电池中,若Cu极生成0. 2 g H2,则电路通过电子0.2NA
③在标准状况下,11.2 L NO与11.2 L O2混合后气体分子数为0.75NA
④常温常压下,16 g O3所含的原子数为NA
⑤1 mol C10H22分子中共价键总数为31NA
⑥1 mol Cl2发生反应时,转移的电子数一定是2NA
⑦标准状况下22. 4 L水中含分子数为NA
A. ①②③④⑤ B. ②④⑤⑥⑦ C. ②④⑤ D. ①②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业制硫酸吸收塔排出的尾气需要处理才能排放到大气中,其处理方法为:先用氨水吸收,再用浓硫酸处理,得到较高浓度的SO2和铵盐。
为测定该铵盐中氮元素的质量分数,将不同质量的铵盐分别加入到50.00mL相同浓度的NaOH溶液中,沸水浴加热至气体全部逸出(此温度下铵盐不分解)。该气体经干燥后用浓硫酸吸收完全,测定浓硫酸增加的质量。
部分测定结果:
铵盐质量为10.00g和20.00g 时,浓硫酸增加的质量相同;铵盐质量为30.00g时,浓硫酸增加的质量为0.68g;铵盐质量为40.00g时,浓硫酸的质量不变。
请计算:
(1)该铵盐中氮元素的质量分数是____%。
(2)若铵盐质量为15.00g,浓硫酸增加的质量为____。(计算结果保留两位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用1 L 1 molL-1Na2SO3溶液吸收SO2时,溶液pH随SO2的物质的量的变化如图所示,下列说法正确的是
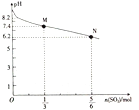
A. 当吸收液呈中性时:c( Na+ ) = c( HSO3-) + 2c(SO32-)
B. M 点时溶液中:c(SO32-)>c(HSO3-)
C. Na2SO3溶液中:c(Na+)>32-)>c(HSO3-)> c(OH-)>c(H+)
D. 向N点的吸收液中加水可使溶液的pH由6. 2升高到7. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组用甲、乙两套装置(如图所示)进行丙烯酸(H2C=CHCOOH)与乙醇(CH3CH2OH)酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃。
回答下列问题:
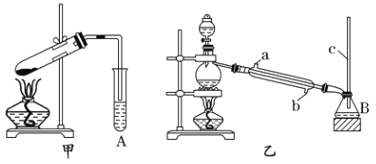
(1)仪器M的名称为_________,仪器A、B中的溶液均为 _________。
(2)甲、乙两套装置中效果比较好的装置是_______,原因是__________。
(3)乙装置中冷凝水应该从______(填“a”或“b”)口进入。
(4)若7.2g丙烯酸与5.2g乙醇完全反应,则理论上生成的丙烯酸乙酯的质量为________。(精确到小数点后一位)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com